题目内容
 KMnO4是一种重要的氧化剂,广泛用于化学分析和化工生产.工业上可由软锰矿(主要成分为MnO2)制备,方法如下:
KMnO4是一种重要的氧化剂,广泛用于化学分析和化工生产.工业上可由软锰矿(主要成分为MnO2)制备,方法如下:①将软锰矿和KOH(s)的混合物于空气中加热熔融,得到K2MnO4;
②用水溶解,滤去残渣,酸化滤液,K2MnO4转化为MnO2和KMnO4;
③除去MnO2,浓缩结晶得到KMnO4晶体.
(1)下列各组物质能用酸性KMnO4溶液鉴别的是
A.FeSO4溶液和MgSO4溶液
B.CH3COOH溶液和H2C2O4溶液
C.SO2和CO2
D.SiO2和Al2O3
(2)用软锰矿制备K2MnO4的化学方程式是
(3)步骤③中除去MnO2的操作名称是
(4)第②步反应的理论产率为
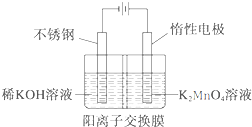
(5)电解法克服了上述过程理论产率偏低的问题,同时副产品KOH可用于软锰矿的焙烧.电解法制备高锰酸钾的实验装置示意图如图(图中阳离子交换膜只允许K+离子通过):
①阳极的电极反应式为
②阴极区生成KOH的原因是
③若电解开始时阳极区溶液为1.0L 0.40mol/L K2MnO4溶液,电解一段时间后,溶液中n(K)/n(Mn)为6:5,阴极区生成KOH的质量为
考点:电解原理,制备实验方案的设计
专题:
分析:(1)根据酸性KMnO4溶液具有强氧化性判断;
(2)MnO2、KOH的熔融混合物中通入空气时发生反应生成K2MnO4,根据元素守恒还应生成水.反应中锰元素由+4价升高为+6价,总升高2价,氧元素由0价降低为-2价,总共降低4价,化合价升降最小公倍数为4,所以MnO2系数2,O2系数为1,根据锰元素守恒确定K2MnO4系数,根据钾元素守恒确定KOH系数,根据氢元素守恒确定H2O系数;
(3)根据MnO2不溶于水分析除去MnO2的操作名称;
(4)由酸化滤液,K2MnO4转化为MnO2和KMnO4,反应为3MnO42-+4H+═MnO2↓+2MnO4-+2H2O,据此计算;
(5)①根据阳极失电子发生氧化反应书写电极反应式;
②根据阴极区反应及其离子移动分析;
③根据阳极区反应,结合题给数据计算阳极区的K+定向移动到阴极区的物质的量,从而计算阴极区生成KOH的质量.
(2)MnO2、KOH的熔融混合物中通入空气时发生反应生成K2MnO4,根据元素守恒还应生成水.反应中锰元素由+4价升高为+6价,总升高2价,氧元素由0价降低为-2价,总共降低4价,化合价升降最小公倍数为4,所以MnO2系数2,O2系数为1,根据锰元素守恒确定K2MnO4系数,根据钾元素守恒确定KOH系数,根据氢元素守恒确定H2O系数;
(3)根据MnO2不溶于水分析除去MnO2的操作名称;
(4)由酸化滤液,K2MnO4转化为MnO2和KMnO4,反应为3MnO42-+4H+═MnO2↓+2MnO4-+2H2O,据此计算;
(5)①根据阳极失电子发生氧化反应书写电极反应式;
②根据阴极区反应及其离子移动分析;
③根据阳极区反应,结合题给数据计算阳极区的K+定向移动到阴极区的物质的量,从而计算阴极区生成KOH的质量.
解答:
解:(1)A.酸性KMnO4溶液具有强氧化性可以氧化FeSO4溶液而使酸性KMnO4溶液退色,不氧化MgSO4溶液,故A正确;
B.酸性KMnO4溶液具有强氧化性可以氧化H2C2O4溶液而使酸性KMnO4溶液退色,不氧化CH3COOH溶液,故B正确;
C.酸性KMnO4溶液具有强氧化性可以氧化SO2而使酸性KMnO4溶液退色,不氧化CO2,故C正确;
D.酸性KMnO4溶液与SiO2和Al2O3都不反应,故不能鉴别,故D错误;
故答案为:ABC;
(2)由信息可知,MnO2、KOH的熔融混合物中通入空气时发生反应生成K2MnO4,根据元素守恒还应生成水.反应中锰元素由+4价升高为+6价,总升高2价,氧元素由0价降低为-2价,总共降低4价,化合价升降最小公倍数为4,所以MnO2系数2,O2系数为1,根据锰元素守恒确定K2MnO4系数为2,根据钾元素守恒确定KOH系数为4,根据氢元素守恒确定H2O系数为2,所以反应化学方程式为2MnO2+4KOH+O2
2K2MnO4+2H2O,
故答案为:2MnO2+4KOH+O2
2K2MnO4+2H2O;
(3)因为MnO2不溶于水,则除去MnO2的操作名称为过滤,故答案为:过滤;
(4)由酸化滤液,K2MnO4转化为MnO2和KMnO4,反应为3MnO42-+4H+═MnO2↓+2MnO4-+2H2O,据此则3MnO42-生成2MnO4-,所以理论产率为
×100%=66.7%,故答案为:66.7%;
(5)①阳极失电子发生氧化反应,所以电极反应式为MnO42--e-=MnO4-;故答案为:MnO42--e-=MnO4-;
②阴极区氢离子得电子发生还原反应,电极反应式为2H2O+2e-═2OH-+H2↑,所以生成氢氧根,又阳极区的K+定向移动到阴极区,所以阴极区生成KOH,故答案为:阴极区发生电极反应2H2O+2e-═2OH-+H2↑,产生OH-,在电流作用下,阳极区的K+定向移动到阴极区;
③根据阳极区反应MnO42--e-=MnO4-,锰原子的物质的量不变,所以仍为1.0L×0.40mol/L=0.4mol,电解一段时间后,溶液中n(K)/n(Mn)为6:5,所以反应后n(K)=0.48mol,则阳极区的K+定向移动到阴极区的物质的量为0.4mol×2-0.48mol=0.32mol,所以阴极生成KOH的物质的质量为0.32mol×56g/mol=17.9 g,
故答案为:17.9 g.
B.酸性KMnO4溶液具有强氧化性可以氧化H2C2O4溶液而使酸性KMnO4溶液退色,不氧化CH3COOH溶液,故B正确;
C.酸性KMnO4溶液具有强氧化性可以氧化SO2而使酸性KMnO4溶液退色,不氧化CO2,故C正确;
D.酸性KMnO4溶液与SiO2和Al2O3都不反应,故不能鉴别,故D错误;
故答案为:ABC;
(2)由信息可知,MnO2、KOH的熔融混合物中通入空气时发生反应生成K2MnO4,根据元素守恒还应生成水.反应中锰元素由+4价升高为+6价,总升高2价,氧元素由0价降低为-2价,总共降低4价,化合价升降最小公倍数为4,所以MnO2系数2,O2系数为1,根据锰元素守恒确定K2MnO4系数为2,根据钾元素守恒确定KOH系数为4,根据氢元素守恒确定H2O系数为2,所以反应化学方程式为2MnO2+4KOH+O2
| ||
故答案为:2MnO2+4KOH+O2
| ||
(3)因为MnO2不溶于水,则除去MnO2的操作名称为过滤,故答案为:过滤;
(4)由酸化滤液,K2MnO4转化为MnO2和KMnO4,反应为3MnO42-+4H+═MnO2↓+2MnO4-+2H2O,据此则3MnO42-生成2MnO4-,所以理论产率为
| 2 |
| 3 |
(5)①阳极失电子发生氧化反应,所以电极反应式为MnO42--e-=MnO4-;故答案为:MnO42--e-=MnO4-;
②阴极区氢离子得电子发生还原反应,电极反应式为2H2O+2e-═2OH-+H2↑,所以生成氢氧根,又阳极区的K+定向移动到阴极区,所以阴极区生成KOH,故答案为:阴极区发生电极反应2H2O+2e-═2OH-+H2↑,产生OH-,在电流作用下,阳极区的K+定向移动到阴极区;
③根据阳极区反应MnO42--e-=MnO4-,锰原子的物质的量不变,所以仍为1.0L×0.40mol/L=0.4mol,电解一段时间后,溶液中n(K)/n(Mn)为6:5,所以反应后n(K)=0.48mol,则阳极区的K+定向移动到阴极区的物质的量为0.4mol×2-0.48mol=0.32mol,所以阴极生成KOH的物质的质量为0.32mol×56g/mol=17.9 g,
故答案为:17.9 g.
点评:本题考查化学反应方程式的书写及有关电解原理的应用和计算,明确反应物与生成物及物质之间的关系是解答的关键,难度不大.

练习册系列答案
相关题目
提纯分离下述物质时,采用的方法与制取无水乙醇的方法相同的是( )
| A、分离硬脂酸和甘油 |
| B、除去乙醛中少量醋酸 |
| C、分离苯酚和苯 |
| D、分离乙烷和乙醇 |
常温下在20mL 0.l mol?L-1 Na2A溶液(pH=11)中逐滴加入0.1mol/L的盐酸,溶液的pH逐渐降低,下列说法一定正确的是(NA表示阿伏加德罗常数)( )
| A、当盐酸加入10mL时,溶液中c(Na+)=2 c(HA-)+2c(A2-)+2 c(H2A) |
| B、当盐酸加入20mL时,溶液中c(Na+)>c(Cl-)>c(HA-)>c(H+)>c(OH-) |
| C、当盐酸加入20mL时,溶液中HA-的数目小于0.002NA |
| D、当盐酸加入40mL时,溶液中c(Na+)+c(H+)=c(OH-)+c(HA-)+c(A2-)+c(Cl-) |
恒温下,向容积为2L的密闭容器中加入MgSO4(s)和CO(g),发生反应:MgSO4(s)+CO(g)
MgO(s)+CO2(g)+SO2(g)反应过程中测定的部分数据见下表:下列说法正确的是( )
| ||
| 反应时间/min | n(MgSO4)/mol | n(CO)/mol | n(CO2)/mol |
| 0 | 2.00 | 2.00 | 0 |
| 2 | 0.80 | ||
| 4 | 1.20 |
| A、反应在0~2min内的平均速率为v(SO2)=0.6 mol?L-l?min-l |
| B、反应在2~4min内容器内气体的密度没有变化 |
| C、若升高温度,反应的平衡常数变为l.00,则正反应为放热反应 |
| D、保持其他条件不变,起始时向容器中充入1.00mol MgSO4和1.00molCO,到达平衡时n(CO2)>0.60mol |
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是周期表中原子半径最小的元素,Y元素的最高正价与最低负价绝对值相等,Z的核电荷数是Y的2倍,W最外层电子数是最内层电子数的3倍.下列说法正确的是( )
| A、微粒半径:Z2+>W2->R- |
| B、对应氢化物的稳定性:W>R |
| C、W与X、W与Z形成的化学物晶体类型相同 |
| D、Y的最高价氧化物对应的水化物是弱酸 |
用NA表示阿伏加德罗常数的值,下列叙述中不正确的是( )
| A、分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA |
| B、1molH2O含有的原子数目为3NA |
| C、常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA |
| D、常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2NA |
化工生产中常用MnS作沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s)?CuS(s)+Mn2+(aq),下列说法错误的是( )
| A、MnS的Ksp比CuS的Ksp大 | ||||
B、该反应达到平衡时:
| ||||
| C、往平衡体系中加入少量CuSO4固体后,c(Mn2+)变大 | ||||
| D、MnS(s)的浊液中加入少量可溶性MnSO4固体后,c(S2-)变大 |