题目内容
8.0.1mol/L的KOH与等浓度等体积的草酸(H2C2O4)溶液混合后,溶液呈酸性,则下列的说法正确的是( )| A. | 溶液呈酸性说明草酸是弱酸 | B. | c(K+)+c(H+)═c(HC2O4-)+c(OH-)+2c(C2O42-) | ||
| C. | c(K+)>c(HC2O4-)>c(C2O42-)>c(H+) | D. | c(H2C2O4)>c(C2O42-) |
分析 草酸为二元酸,0.1mol/L的KOH与等浓度等体积的草酸(H2C2O4)溶液混合,可生成KHC2O4,溶液呈酸性,说明溶液呈酸性电离程度大于水解程度,结合电荷守恒解答该题.
解答 解:A.由于草酸为二元酸,与KOH反应时操作过量,不能说明草酸为弱酸,该A错误;
B.反应生成1KHC2O4,根据电荷守恒可知:c(K+)+c(H+)=c(HC2O4-)+2c(C2O42-)+c(OH-),故B正确;
C.因还存在水的电离,则c(H+)>c(C2O42-),故C错误;
D.KHC2O4溶液中,溶液呈酸性,说明HC2O4-电离程度大于其水解程度,则c(C2O42-)>c(H2C2O4),故D错误.
故选B.
点评 本题考查了离子浓度大小比较,为高频考点,侧重于学生的分析能力的考查,题目难度中等,注意掌握电荷守恒、物料守恒在判断离子浓度大小中的应用方法.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
18.X、Y、Z、W、R属于短周期主族元素.X的原子半径是短周期主族元素中最大的,Y元素的单质通过分离液态空气得到,Z元素的单质是常见的半导体材料,W与Z同族,R与Y同族,其单质有杀菌作用.下列叙述不正确的是
( )
( )
| A. | 与Z同族的第五周期元素的原子序数为50 | |
| B. | Y的简单氢化物的沸点和热稳定性均大于R的简单氢化物 | |
| C. | X与Y形成的两种化合物中阴、阳离子的个数比均为1:2,且均能与水反应 | |
| D. | 由W和Z组成的ZW物质硬度大、熔沸点高,具有导磁性 |
19.密度为0.910g/cm3的氨水,质量分数为25.0%,该氨水用等体积的水稀释后,所得溶液的质量分数为( )
| A. | 等于12.5% | B. | 大于12.5% | C. | 小于12.5% | D. | 无法确定 |
16.除去下列物质中的杂质(括号内为杂质),所选用的试剂及操作方法正确的是( )
| 选项 | 待提纯的物质 | 选用试剂 | 操作的方法 |
| A | FeCl3溶液(FeCl2溶液) | 铜粉 | 过滤 |
| B | CO2(SO2) | NaHCO3溶液 | 洗气 |
| C | HCl(Cl2) | 饱和食盐水 | 洗气 |
| D | NH4Cl固体(I2固体) | -- | 加热至质量不再变化 |
| A. | A | B. | B | C. | C | D. | D |
13.下列各组物质分类中,按物质的分类后者从属于前者的是( )
| A. | 金属、非金属、稀有气体 | B. | 化合物、盐、酸式盐 | ||
| C. | 碱、碱性氧化物、碱式盐 | D. | 混合物、化合物、纯净物 |
17.与50mL 0.1mol/L的Na2CO3溶液中Na+的物质的量浓度相同的溶液是( )
| A. | 100 mL 0.2 mol/L的NaCl溶液 | B. | 100 mL 0.1 mol/L的NaCl溶液 | ||
| C. | 25 mL 0.2 mol/L的Na2SO4溶液 | D. | 50 mL 0.1 mol/L的NaHCO3溶液 |
18.下列选项中,错误的是( )
| A. | 需要加快反应速率的过程是炼钢 | |
| B. | 世界上第一张元素周期表的作者是门捷列夫 | |
| C. | 乙烯与溴的四氯化碳溶液反应的类型为取代反应 | |
| D. | 在葡萄糖溶液中加入新制的Cu(OH)2,加热煮沸后产生沉淀的颜色为砖红色 |
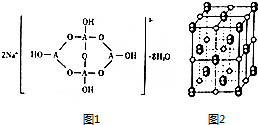 已知A、B、C、D、E五种元素是周期表中前四周期元素,且原子序数依次增大.其中A、B、C为同周期的非金属元素,且B、C原子中均有两个未成对电子.D、E为同周期元素且分别位于s区和d区.五种元素所有的s能级电子均为全充满.E的d能级电子数等于A、B、C最高能层的p能级电子数之和.回答下列问题:
已知A、B、C、D、E五种元素是周期表中前四周期元素,且原子序数依次增大.其中A、B、C为同周期的非金属元素,且B、C原子中均有两个未成对电子.D、E为同周期元素且分别位于s区和d区.五种元素所有的s能级电子均为全充满.E的d能级电子数等于A、B、C最高能层的p能级电子数之和.回答下列问题: .
.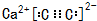 ,若晶胞的长宽高分别为520pm、520pm和690pm,该晶体密度为2.28g/cm3(保留到小数点后两位).
,若晶胞的长宽高分别为520pm、520pm和690pm,该晶体密度为2.28g/cm3(保留到小数点后两位).