题目内容
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、50mL 18.4mol?L-1浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA |
| B、常温常压下,4.6gNO2与N2O4混合气中含有0.3NA个原子 |
| C、1L0.1mol?L-1Na2CO3溶液中含有的阴离子数为0.1NA |
| D、标准状况下,22.4LCCl4中含有NA个分子 |
考点:阿伏加德罗常数
专题:
分析:A、浓硫酸随反应进行,浓度会逐渐减小为稀硫酸,此时则不与铜发生反应;
B、根据NO2和N2O4混合气体的最简式进行计算所含原子总数;
C、常温下,1L0.1mol?L-1 Na2CO3溶液中,碳酸根离子部分水解生成氢氧根离子和碳酸氢根离子,导致溶液中阴离子数目增多;
D、标况下,四氯化碳为液态.
B、根据NO2和N2O4混合气体的最简式进行计算所含原子总数;
C、常温下,1L0.1mol?L-1 Na2CO3溶液中,碳酸根离子部分水解生成氢氧根离子和碳酸氢根离子,导致溶液中阴离子数目增多;
D、标况下,四氯化碳为液态.
解答:
解:A、浓硫酸随反应进行,浓度减小为稀硫酸不与铜发生反应,生成SO2分子数目小于0.46NA,故A错误;
B、NO2和N2O4混合气体的最简式为NO2,4.6g混合气体含有0.1mol最简式NO2,含有0.3mol原子,所含原子总数为0.3NA,故B正确;
C、常温下,1L0.1mol?L-1 Na2CO3溶液中含有溶质碳酸钠0.1mol,由于碳酸根离子部分水解,导致溶液中阴离子大于0.1mol,溶液中阴离子数目之和大于0.1NA,故C错误;
D、标况下,四氯化碳为液态,故D错误.
故选B.
B、NO2和N2O4混合气体的最简式为NO2,4.6g混合气体含有0.1mol最简式NO2,含有0.3mol原子,所含原子总数为0.3NA,故B正确;
C、常温下,1L0.1mol?L-1 Na2CO3溶液中含有溶质碳酸钠0.1mol,由于碳酸根离子部分水解,导致溶液中阴离子大于0.1mol,溶液中阴离子数目之和大于0.1NA,故C错误;
D、标况下,四氯化碳为液态,故D错误.
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
25℃时,0.1mol/L稀醋酸加水稀释,如图中的纵坐标y可以是( )
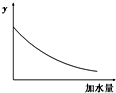

| A、溶液的pH |
| B、醋酸的电离平衡常数 |
| C、醋酸的电离程度 |
| D、溶液的导电能力 |
下列有关化学用语的表示正确的是( )
| A、HClO的结构式:H-Cl-O |
| B、硝基和二氧化氮两种粒子所含电子数相等 |
C、甲烷分子的比例模型是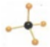 |
D、甲基的电子式: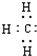 |
下列物质属于纯净物的是( )
| A、稀硫酸 | B、NaOH |
| C、液化石油气 | D、天然气 |
用NA表示阿伏伽德罗常数,以下说法正确的是( )
| A、1 mol乙烷中的氢原子被氯原子完全取代,需要氯气分子数为 4 NA |
| B、1 mol的NO2 与水完全反应转移电子数为NA |
| C、在标准状况下2.24 L O2 和3.2 g O3含有氧原子都为0.2 NA. |
| D、在标准状况下2.24 L丙烷和戊烷混合物含分子个数为0.1 NA. |
搜狐网曾报道,中国每年要进口5亿吨左右的铁矿石,占世界海上铁矿石贸易量的一半以上,随着全球铁矿石价格的上涨,中国钢铁工业协会与澳大利亚必和必拓公司谈判陷入困境,关于铁矿石说法正确的是( )
| A、赤铁矿的主要成分是Fe3O4 |
| B、铁矿石的主要成分与铁锈的主要成分相同 |
| C、磁铁矿粉末溶于盐酸后,加入KSCN溶液,溶液变红色 |
| D、FeO俗称铁红 |
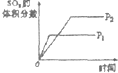


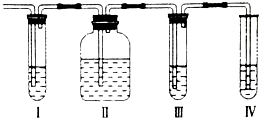 在实验室里制取的乙烯中常混有少量的二氧化硫,某化学兴趣小组设计了如图所示的实验装置以确认上述混合气体中是否含有SO2和C2H4.请回答下列问题:
在实验室里制取的乙烯中常混有少量的二氧化硫,某化学兴趣小组设计了如图所示的实验装置以确认上述混合气体中是否含有SO2和C2H4.请回答下列问题: