题目内容
9.由锌、铁、铝、镁四种金属中的两种组成的混合物23g,与足量的盐酸反应产生的氢气标准状况下为22.4L,则两种金属组成的混合物可能是( )| A. | 锌与镁 | B. | 铁与锌 | C. | 铝与铁 | D. | 镁与铁 |
分析 若均为+2价金属,与盐酸反应氢气,存在M~H2↑,n(H2)=$\frac{22.4L}{22.4L/mol}$=1mol,则金属的平均相对摩尔质量为$\frac{23g}{1mol}$=23g/mol,结合平均值法来解答.
解答 解:若均为+2价金属,与盐酸反应氢气,存在M~H2↑,n(H2)=$\frac{22.4L}{22.4L/mol}$=1mol,则金属的平均相对摩尔质量为$\frac{23g}{1mol}$=23g/mol,
A.Zn、Mg的相对原子质量分别为65、24,均大于23,故A不选;
B.Fe、Zn的相对原子质量分别为56、65,均大于23,故B不选;
C.Al转化为+2价时其相对原子质量为27×$\frac{2}{3}$=18,Fe的相对原子质量为56,则平均值可为23,故C选;
D.Mg、Fe的相对原子质量分别为24、56,均大于23,故D不选;
故选C.
点评 本题考查金属与酸的反应,为高频考点,把握+2价金属与酸反应的规律及平均值为解答的关键,侧重分析与计算能力的考查,注意平均值法的应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.下列有关物质的性质与用途具有对应关系的是( )
| A. | MgO、Al2O3熔点高,均可用作耐高温材料 | |
| B. | NH4HCO3受热易分解,可用作氮肥 | |
| C. | Fe2(SO4)3易溶于水,可用作净水剂 | |
| D. | SO2具有氧化性,可用于漂白纸浆 |
20.下列说法不能证明CH3COOH是弱酸的是( )
| A. | CH3COOH溶液的导电能力比相同浓度的HCl溶液小 | |
| B. | 在25℃时,0.1mol/L的CH3COOH溶液pH约为3 | |
| C. | 在25℃时,1mol/L的CH3COONa溶液的pH约为9 | |
| D. | 0.1molCH3COOH和0.1 mol NaOH恰好中和生成CH3COONa |
17.下列反应的离子方程式书写正确的是( )
| A. | 将Al条投入NaOH溶液中:Al+4OH-=AlO2-+2H2O | |
| B. | 铜溶于浓硫酸中并加热:Cu+4H++SO42-$\frac{\underline{\;\;△\;\;}}{\;}$Cu2++SO2↑+2H2O | |
| C. | 碳酸氢钙溶液中加入少量氢氧化钙溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O | |
| D. | 向碳酸钠溶液中逐滴加入与之等体积等物质的量浓度的稀硫酸:CO32-+H+=HCO3- |
4.下列有机物中含有( )种官能团
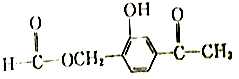

| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
14.将100gNa2CO3和NaHCO3的混合物用酒精灯加热至质量不再变化时,固体质量减少到75.2g.此混合物中Na2CO3的质量分数是( )
| A. | 75.2% | B. | 67.2% | C. | 41.7% | D. | 32.8% |
1.下列叙述Ⅰ和Ⅱ均正确并有因果关系的是( )
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | Si有导电性 | Si可用于制备光导纤维 |
| B | Fe的金属活动性大于Cu | FeCl3溶液可用于回收废旧电路板中的铜 |
| C | Na2O2与水反应能生成碱 | Na2O2属于碱性氧化物 |
| D | 次氯酸光照易分解 | 新制氯水保存在棕色试剂瓶中,放于冷暗处 |
| A. | A | B. | B | C. | C | D. | D |
18.若已知反应 NaNO2+HF═HNO2+NaF,7.2×10-4、4.6×10-4分别是上式所涉及的两种酸的电离常数.由此可判断下列叙述中不正确的是( )
| A. | K(HF)=c(F-)?c(H+)/c(HF ) | B. | K(HNO2)=7.2×10-4 | ||
| C. | 酸性强弱为 HF>HNO2 | D. | K(HNO2)<K(HF) |
 我国规定:室内甲醛含量不得超过0.08mg•m-3.某研究性学习小组欲利用酸性KMnO4溶液测定空气中甲醛的含量,请你协助他们完成相关学习任务.(部分装置如图),其反应原理及步骤如下:
我国规定:室内甲醛含量不得超过0.08mg•m-3.某研究性学习小组欲利用酸性KMnO4溶液测定空气中甲醛的含量,请你协助他们完成相关学习任务.(部分装置如图),其反应原理及步骤如下: