题目内容
已知:等浓度的CH3COOH和NH3?H2O电离程度相当,氢氧化镁能溶于浓度均为3mol/L的下列溶液中:①盐酸 ②NH4Cl溶液 ③醋酸铵溶液,下列说法正确的是( )
| A、c(NH4+):③>② |
| B、pH:①>②>③ |
| C、Mg(OH)2溶于②的主要原因是由于NH4+水解使溶液显酸性,导致平衡Mg(OH)2(s)═Mg2+(aq)+2OH-(aq)向溶解方向移动 |
| D、等体积 ①和 ③混合溶液中 c(Cl-)>c(NH4+)>c(H+)>c(CH3COO-)>c(OH-) |
考点:pH的简单计算,难溶电解质的溶解平衡及沉淀转化的本质,离子浓度大小的比较
专题:
分析:A.醋酸根离子促进铵根离子水解,铵根离子水解程度越大,溶液中c(NH4+)越小;
B.HCl溶液呈强酸性,氯化铵溶液呈弱酸性,醋酸铵溶液呈中性,据此判断pH大小;
C.NH4++OH-?NH3.H2O,从而促进Mg(OH)2溶解;
D.等体积等浓度的①和③混合,二者反应生成等物质的量浓度的氯化铵和醋酸,溶液呈酸性,且醋酸电离程度大于铵根离子水解程度.
B.HCl溶液呈强酸性,氯化铵溶液呈弱酸性,醋酸铵溶液呈中性,据此判断pH大小;
C.NH4++OH-?NH3.H2O,从而促进Mg(OH)2溶解;
D.等体积等浓度的①和③混合,二者反应生成等物质的量浓度的氯化铵和醋酸,溶液呈酸性,且醋酸电离程度大于铵根离子水解程度.
解答:
解:A.铵根离子水解程度越大,溶液中c(NH4+)越小,醋酸根离子促进铵根离子水解,所以c(NH4+):③<②,故A错误;
B.HCl溶液呈强酸性,氯化铵溶液呈弱酸性,醋酸铵溶液呈中性,则三种溶液pH大小顺序为;③>②>①,故B错误;
C.NH4Cl中含有铵根离子,Mg(OH)2能电离出OH-,NH4++OH-?NH3.H2O,从而促进Mg(OH)2溶解,故C错误;
D.等体积等浓度的①和③混合,二者反应生成等物质的量浓度的氯化铵和醋酸,溶液呈酸性,且醋酸电离程度大于铵根离子水解程度,结合物料守恒得离子浓度大小顺序是:c(Cl-)>c(NH4+)>c(H+)>c(CH3COO-)>c(OH-),故D正确;
故选D.
B.HCl溶液呈强酸性,氯化铵溶液呈弱酸性,醋酸铵溶液呈中性,则三种溶液pH大小顺序为;③>②>①,故B错误;
C.NH4Cl中含有铵根离子,Mg(OH)2能电离出OH-,NH4++OH-?NH3.H2O,从而促进Mg(OH)2溶解,故C错误;
D.等体积等浓度的①和③混合,二者反应生成等物质的量浓度的氯化铵和醋酸,溶液呈酸性,且醋酸电离程度大于铵根离子水解程度,结合物料守恒得离子浓度大小顺序是:c(Cl-)>c(NH4+)>c(H+)>c(CH3COO-)>c(OH-),故D正确;
故选D.
点评:本题考查了弱电解质的电离和盐类水解、难溶物的溶解平衡等知识点,题目难度中等,会正确分析氢氧化镁溶于氯化铵的原因,很多同学往往认为氯化铵水解生成的盐酸溶解氢氧化镁而导致错误,为易错点.

练习册系列答案
相关题目
在2A+B?3C+4D反应中,表示该反应速率最快的是( )
| A、v(A)=0.5 mol/(L?s) |
| B、v(B)=0.3 mol/(L?s) |
| C、v(C)=0.8 mol/(L?s) |
| D、v(D)=1 mol/(L?s) |
溶液、胶体和浊液这三种分散系的根本区别是( )
| A、是否均一、稳定、透明 |
| B、分散质微粒直径的大小 |
| C、能否透过滤纸 |
| D、分散质的粒子是否为大量分子或离子的集合体 |
用0.1mol/LNaOH溶液滴定0.1mol/L盐酸溶液,如达到滴定终点时不慎多加了1滴NaOH溶液 (1滴溶液的体积约为0.05mL),继续加水至50mL,所得溶液的pH是( )
| A、10 | B、9 |
| C、11.5 | D、12.5 |
 某溶液中可能含有,OH-、CO32-,AlO2-,SiO32-,SO42-,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图.下列判断正确的是( )
某溶液中可能含有,OH-、CO32-,AlO2-,SiO32-,SO42-,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图.下列判断正确的是( )| A、原溶液中一定含有Na2SO4 |
| B、原溶液中一定含有的阴离子是OH-,CO32-,SiO32-,AlO2- |
| C、反应后形成的溶液溶质为NaCl |
| D、原溶液中含有CO32-与AlO2-的物质的量比为1:2 |
 氮元素可形成卤化物、叠氮化物及络合物等.
氮元素可形成卤化物、叠氮化物及络合物等.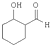 子式
子式 1mol最多能与
1mol最多能与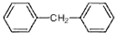 中,共平面的碳原子最多有
中,共平面的碳原子最多有