题目内容
铁是人体必需的微量元素,人体内缺乏铁元素会引起缺铁性贫血,需要补充铁质,目前市售补铁制品较多,为保护消费者的利益,质检部门需对补铁剂中铁的含量进一步测定,测定步骤如下:
(1)将补铁剂中的Fe2+用H2O2转变成Fe3+,加入H2O2的目的是 ,若不用H2O2,可以用 .
(2)根据你所学过的知识,写出检验Fe3+的化学试剂和实验现象:
(3)将Fe3+用氨水沉淀,试写出发生的离子方程式 .
(4)过滤,将沉淀灼烧得红褐色固体,称量.试写出发生的化学方程式 .
(1)将补铁剂中的Fe2+用H2O2转变成Fe3+,加入H2O2的目的是
(2)根据你所学过的知识,写出检验Fe3+的化学试剂和实验现象:
(3)将Fe3+用氨水沉淀,试写出发生的离子方程式
(4)过滤,将沉淀灼烧得红褐色固体,称量.试写出发生的化学方程式
考点:铁的化学性质,铁盐和亚铁盐的相互转变,二价Fe离子和三价Fe离子的检验
专题:几种重要的金属及其化合物
分析:(1)双氧水具有氧化性,酸性条件下能将Fe2+全部氧化为Fe3+,和其它的氧化剂如O3、酸性高锰酸钾、新配制的氯水;
(2)检验Fe3+的化学试剂KSCN溶液,硫氰化钾溶液与铁离子反应,溶液显示红色,可以检验溶液中是否含有铁离子;
(3)将Fe3+用氨水沉淀,方程式为Fe3++3NH3.H2O=Fe(OH)3↓+3NH4+;
(4)将沉淀灼烧得红褐色固体,方程式为2Fe(OH)3=Fe2O3+3H2O.
(2)检验Fe3+的化学试剂KSCN溶液,硫氰化钾溶液与铁离子反应,溶液显示红色,可以检验溶液中是否含有铁离子;
(3)将Fe3+用氨水沉淀,方程式为Fe3++3NH3.H2O=Fe(OH)3↓+3NH4+;
(4)将沉淀灼烧得红褐色固体,方程式为2Fe(OH)3=Fe2O3+3H2O.
解答:
解:(1)双氧水具有氧化性,酸性条件下能将Fe2+全部氧化为Fe3+,和其它的氧化剂如O3、酸性高锰酸钾、新配制的氯水,故答案为:酸性条件下能将Fe2+全部氧化为Fe3+;O3、酸性高锰酸钾、新配制的氯水;
(2)检验Fe3+的化学试剂KSCN溶液,故答案为:硫氰化钾溶液与铁离子反应,溶液显示红色,可以检验溶液中是否含有铁离子;
(3)将Fe3+用氨水沉淀,方程式为Fe3++3NH3.H2O=Fe(OH)3↓+3NH4+,故答案为:Fe3++3NH3.H2O=Fe(OH)3↓+3NH4+;
(4)将沉淀灼烧得红褐色固体,方程式为2Fe(OH)3=Fe2O3+3H2O,故答案为:2Fe(OH)3=Fe2O3+3H2O.
(2)检验Fe3+的化学试剂KSCN溶液,故答案为:硫氰化钾溶液与铁离子反应,溶液显示红色,可以检验溶液中是否含有铁离子;
(3)将Fe3+用氨水沉淀,方程式为Fe3++3NH3.H2O=Fe(OH)3↓+3NH4+,故答案为:Fe3++3NH3.H2O=Fe(OH)3↓+3NH4+;
(4)将沉淀灼烧得红褐色固体,方程式为2Fe(OH)3=Fe2O3+3H2O,故答案为:2Fe(OH)3=Fe2O3+3H2O.
点评:本题考查了铁离子的检验方法,离子方程式和化学方程式的书写,题目难度不大,注意熟练掌握常见离子的检验方法.

练习册系列答案
相关题目
实验室从碘水中提取碘的主要操作,正确的是( )
| A、蒸馏 | B、过滤 | C、分液 | D、萃取 |
酸雨的形成主要是由于( )
| A、森林遭到乱砍滥伐,破坏了生态平衡 |
| B、工业上大量燃烧含硫燃料 |
| C、氟氯烃的大量排放 |
| D、大气中二氧化碳含量增多 |
下列属于强电解质的是( )
| A、醋酸 | B、酒精 | C、铜 | D、小苏打 |
如图是物质分类的一部分:其中所举例的物质错误的是( )
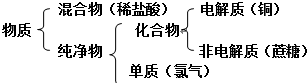

| A、稀盐酸 | B、铜 | C、蔗糖 | D、氯气 |
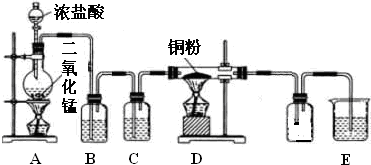
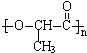 ,则形成该高聚物的单体结构简式为
,则形成该高聚物的单体结构简式为