题目内容
(6分)臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压放电管来制取臭氧:3O22O3。
(1)若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为多少?(保留一位小数)。
(2)将8 L氧气通过放电管后,恢复到原状况,得到气体6.5 L,其中臭氧的体积为多少升?
(3)实验室将氧气和臭氧的混合气体0.896 L(标准状况)通入盛有20.0 g铜粉的反应器中,充分加热后,粉末的质量变为21.6 g。则原混合气中臭氧的体积分数为多少?
(1)35.6g/mol (2)3L (3)0.5
【解析】(1)设氧气的物质的量是1mol,则根据反应式3O22O3可知,生成臭氧是0.2mol,所以混合气的平均摩尔质量为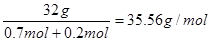 。
。
(2)3O22O3 △V
3 2 1
3 (8-6.5)
即臭氧的体积为3L。
(3)n(混合气体)==0.04 mol
设臭氧的体积分数为a,根据氧原子守恒
0.04 mol×a×3+0.04 mol×(1-a)×2=
解得a=0.5

 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
| |||||||||||||||||||||||||||||||