题目内容
下列各组物质中,所含分子数相同的是( )
| A、10g H2和10g O2 |
| B、7g N2和11g CO2 |
| C、9g H2O和0.5mol Br2 |
| D、224mL H2(标准状况)和0.1mol N2 |
考点:物质的量的相关计算
专题:计算题
分析:根据n=
=
计算各气体的物质的量,物质的量相同,则分子数相同,据此分析.
| m |
| M |
| V |
| Vm |
解答:
解:A.10g H2物质的量=
=5mol;10g O2 物质的量=
=0.3125mol,物质的量不同分子数不同,故A错误;
B.7g N2物质的量=
=0.25mol,11g CO2物质的量=
=0.25mol,物质的量相同分子数相同,故B正确;
C.9g H2O的物质的量=
=0.5mol和0.5mol Br2,物质的量相同分子数相同,故C正确;
D.224mL H2(标准状况)的物质的量=
=0.01mol和0.1mol N2,物质的量不同分子数不同,故D错误.
故选BC.
| 10g |
| 2g/mol |
| 10g |
| 32g/mol |
B.7g N2物质的量=
| 7g |
| 28g/mol |
| 11g |
| 44g/mol |
C.9g H2O的物质的量=
| 9g |
| 18g/mol |
D.224mL H2(标准状况)的物质的量=
| 0.224L |
| 22.4L/mol |
故选BC.
点评:本题考查了物质的量和各量的计算关系分析应用,注意分子数相同是指微粒物质的量相同,题目较简单.

练习册系列答案
相关题目
已知NaHSO3溶液显酸性,溶液中存在以下平衡:
HSO3-+H2O?H2SO3+OH- ①
HSO3-?H++SO32- ②
向0.1mol?L-1的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是( )
HSO3-+H2O?H2SO3+OH- ①
HSO3-?H++SO32- ②
向0.1mol?L-1的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是( )
| A、加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO3-)增大 | ||||||||
| B、加入少量Na2SO3固体,则c(H+)+c(Na+)=c(HSO3-)+c(OH-)+0.5c(SO32-) | ||||||||
C、加入少量NaOH溶液,
| ||||||||
D、加入氨水至中性,则2c(Na+)=c(SO
|
如图是制作一个简单的氢氧燃料电池的实验装置,下列说法中正确的是( )

| A、实验前应先将石墨电极在高温火焰上灼烧,然后浸入冷水处理 |
| B、实验时先将S1、S2同时闭合,通电一段时间后,断开S1 |
| C、实验时可以向溶液中加入NaCl以增强导电性 |
| D、可以在两极分别通入氢气和氧气,以获得较大的电流 |
某种煤气的组成是:50%氢气、30%甲烷、10%一氧化碳、6%氮气和4%二氧化碳(均为体积分数).已知:
2H2(g)+O2(g)=2H2O (l)△H=-571.6kJ?mol-1
2CO(g)+O2(g)=2CO2(g)△H=-565.2kJ?mol-1
CH4(g)+2O2(g)=CO2(g)+H2O(l)△H=-890.3kJ?mol-1
则在标准状况下,224L该种煤气燃烧时放出的热量为( )
2H2(g)+O2(g)=2H2O (l)△H=-571.6kJ?mol-1
2CO(g)+O2(g)=2CO2(g)△H=-565.2kJ?mol-1
CH4(g)+2O2(g)=CO2(g)+H2O(l)△H=-890.3kJ?mol-1
则在标准状况下,224L该种煤气燃烧时放出的热量为( )
| A、2027.1kJ |
| B、4382.5 kJ |
| C、5094.1 kJ |
| D、5811.5 kJ |
下列变化中,一定不存在化学能与热能相互转化的是( )
| A、铝热反应 | B、白磷自燃 |
| C、燃放爆竹 | D、干冰气化 |
下列各项表达式正确的是( )
A、N2的电子式: |
B、H2O2的电子式: |
C、NaCl的电子式: |
D、F-的结构示意图: |

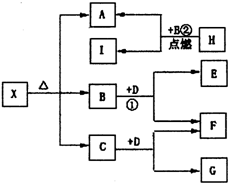 已知X是一种盐,H是常见金属单质,F、I是常见非金属单质,E、G都是工业上重要的碱性物质,它们有如图所示的关系.
已知X是一种盐,H是常见金属单质,F、I是常见非金属单质,E、G都是工业上重要的碱性物质,它们有如图所示的关系.