题目内容
(1)用18mol/L浓硫酸配制100mL 1.0mol/L的稀硫酸,若实验仪器有:
A.100mL量筒 B.玻璃棒 C.托盘天平 D.50mL容量瓶
E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
实验时必须选用的仪器是(填入字母)
(2)在配制过程中,下列操作不正确的是
A.使用容量瓶前需检查它是否漏水
B.将蒸馏水注入容量瓶中,液面离刻度线下1~2cm时,改用胶头滴管滴加至液面与刻度线相切
C.配制溶液时,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水至刻度线
D.定容后盖好瓶塞,反复上下颠倒,摇匀
(3)若实验时遇到下列情况,将使所配溶液的浓度偏高的是
A.定容时仰视读数
B.定容摇匀后,发现液面低于刻度线,再加入蒸馏水至与刻度线相切
C.洗涤量筒,并将洗涤液转入容量瓶
D.在配制前用稀硫酸润洗容量瓶后,未用蒸馏水洗涤.
A.100mL量筒 B.玻璃棒 C.托盘天平 D.50mL容量瓶
E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
实验时必须选用的仪器是(填入字母)
(2)在配制过程中,下列操作不正确的是
A.使用容量瓶前需检查它是否漏水
B.将蒸馏水注入容量瓶中,液面离刻度线下1~2cm时,改用胶头滴管滴加至液面与刻度线相切
C.配制溶液时,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水至刻度线
D.定容后盖好瓶塞,反复上下颠倒,摇匀
(3)若实验时遇到下列情况,将使所配溶液的浓度偏高的是
A.定容时仰视读数
B.定容摇匀后,发现液面低于刻度线,再加入蒸馏水至与刻度线相切
C.洗涤量筒,并将洗涤液转入容量瓶
D.在配制前用稀硫酸润洗容量瓶后,未用蒸馏水洗涤.
考点:配制一定物质的量浓度的溶液
专题:实验题
分析:(1)根据溶液稀释定律C浓V浓=C稀V稀计算出所需的浓硫酸的体积,然后据此选择合适的量筒;根据操作步骤有计算、量取、稀释、洗涤、定容、摇匀等操作来分析所需的仪器;
(2)根据溶液的配制操作来分析;
(3)根据c=
并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析.
(2)根据溶液的配制操作来分析;
(3)根据c=
| n |
| V |
解答:
解:(1)设需要的浓硫酸的体积为XmL,根据溶液稀释定律C浓V浓=C稀V稀可知:18mol/L×XmL=100mL×1.0mol/L,解得X=5.6mL,故应选择10mL量筒.
操作步骤有计算、量取、稀释、洗涤、定容、摇匀等操作,一般用10mL量筒量取浓硫酸,在烧杯中稀释(可用量筒量取水加入烧杯),并用玻璃棒搅拌.冷却后转移到100mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以所需仪器有10mL量筒、烧杯、玻璃棒、100mL容量瓶、胶头滴管,故答案为:BEFGH;
(2)A.容量瓶前需检查它是否漏水,故A正确;
B.容量瓶只能用来配制溶液,不能在容量瓶中溶解或稀释,将蒸馏水注入容量瓶中,液面离刻度线下1-2cm时,改用胶头滴管滴加至液面与刻度线相切,故B正确;
C.量筒量取后应先在小烧杯中稀释,然后将洗涤液一并转入容量瓶,故C错误;
D.定容后需要上下摇匀,故D正确.
故选C;
(3)A.定容时仰视读数,会导致溶液体积偏大,则浓度偏小,故A不选;
B.定容摇匀后,发现液面低于刻度线是正常的,再加入蒸馏水至与刻度线相切会导致浓度偏小,故B不选;
C.量筒为流量式仪器,将量筒洗涤后的洗涤液不能转移至容量瓶,否则会导致容量瓶内硫酸的物质的量增多,浓度偏高,故C选;
D.在配制前用稀硫酸润洗容量瓶后,未用蒸馏水洗涤,容量瓶内硫酸增多,浓度偏高,故D选.
故选CD.
操作步骤有计算、量取、稀释、洗涤、定容、摇匀等操作,一般用10mL量筒量取浓硫酸,在烧杯中稀释(可用量筒量取水加入烧杯),并用玻璃棒搅拌.冷却后转移到100mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以所需仪器有10mL量筒、烧杯、玻璃棒、100mL容量瓶、胶头滴管,故答案为:BEFGH;
(2)A.容量瓶前需检查它是否漏水,故A正确;
B.容量瓶只能用来配制溶液,不能在容量瓶中溶解或稀释,将蒸馏水注入容量瓶中,液面离刻度线下1-2cm时,改用胶头滴管滴加至液面与刻度线相切,故B正确;
C.量筒量取后应先在小烧杯中稀释,然后将洗涤液一并转入容量瓶,故C错误;
D.定容后需要上下摇匀,故D正确.
故选C;
(3)A.定容时仰视读数,会导致溶液体积偏大,则浓度偏小,故A不选;
B.定容摇匀后,发现液面低于刻度线是正常的,再加入蒸馏水至与刻度线相切会导致浓度偏小,故B不选;
C.量筒为流量式仪器,将量筒洗涤后的洗涤液不能转移至容量瓶,否则会导致容量瓶内硫酸的物质的量增多,浓度偏高,故C选;
D.在配制前用稀硫酸润洗容量瓶后,未用蒸馏水洗涤,容量瓶内硫酸增多,浓度偏高,故D选.
故选CD.
点评:本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,难度不大.

练习册系列答案
相关题目
下面有关Na2CO3与NaHCO3的说法正确的是( )
| A、热稳定性:NaHCO3>Na2CO3 |
| B、相同浓度溶液的碱性:Na2CO3<NaHCO3 |
| C、都能与酸反应放出CO2,但剧烈程度:NaHCO3>Na2CO3 |
| D、Na2CO3不能转化成NaHCO3,而NaHCO3能转化成Na2CO3 |
据报道用Mg与石墨作电极与NH4Cl溶液形成原电池(盐桥为装有琼胶的饱和KCl溶液),也可生成NH3.下列说法正确是( )
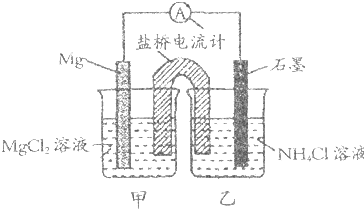

| A、石墨电极反应式为2NH4++2e-=2NH3↑+H2↑ |
| B、乙烧杯中一直存在:c(Cl-)<c(NH4+) |
| C、电子流向是由石墨→导线→Mg |
| D、盐桥中的Cl-移向乙烧杯 |
室温下,取O.2mol/L H2A溶液与xmol/L NaOH溶液等体积混合(忽略混合后溶液体积变化),测得混合溶液的pH=y,下列推断不正确的是( )
| A、当x=0.2,则混合溶液中y可能大于7或小于7 |
| B、当x=0.2,y=1,则混合溶液中:c(H+)=c(A2-)+c(OH-) |
| C、当x=0.3,y>7,则混合溶液中:c(Na+)>c(A2-)>c(HA-)>c(OH-)>c(H+) |
| D、当x=0.4,则混合溶液中:[c(Na+)+c(H+)]>2c(A2-) |
下列除去杂质(试样中括号内的物质是杂质)时,选用的试剂正确的是( )
| A | B | C | D | |
| 试样 | Na2CO3(NaHCO3) | FeCl2(FeCl3) | Fe(A1) | Cl2(HCl) |
| 除杂试剂 | 澄清石灰水 | NaOH溶液 | NaOH溶液 | 饱和NaHCO3溶液 |
| A、A | B、B | C、C | D、D |
能将化学能转化为电能的装置(烧杯中溶液均为稀硫酸)是( )
A、 |
B、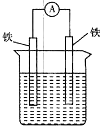 |
C、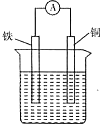 |
D、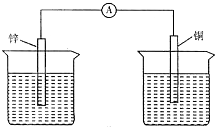 |
