题目内容
17.关于图示两个装置的说法正确的是( )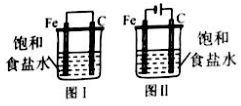
| A. | 两个装置中Fe棒上发生的反应相同 | |
| B. | 图 I中铁比图 II中铁腐蚀更快 | |
| C. | 两个装置中C棒上均明显有气体逸出 | |
| D. | 两个装置中Fe均是负极 |
分析 图1为原电池,铁为负极,铁发生吸氧腐蚀,图2为电解池,铁为阴极,碳棒为阳极,阳极发生氧化反应生成氯气,阴极生成氢气,以此解答该题.
解答 解:A.图1铁为负极,发生氧化反应,图2铁为阴极,发生还原反应,故A错误;
B.图1为吸氧腐蚀,图2为铁的外加电源的阴极保护法,故B正确;
C.图1碳棒发生氧气得到电子的还原反应,没有气体生成,故C错误;
D.图2铁为阴极,故D错误.
故选B.
点评 本题考查原电池、电解池知识,为高频考点,侧重于学生的分析能力的考查,注意把握电极的判断和电极方程式的书写,把握金属的腐蚀以及防护措施,难度不大,注意把握装置的工作原理.

练习册系列答案
相关题目
6.在给定的条件下,下列选项所示的物质间均能通过一步转化实现的是( )
| A. | Fe$→_{高温}^{H_{2}O(g)}$Fe2O3$→_{高温}^{Al}$Al2O3 | |
| B. | Cu$→_{点燃}^{Cl_{2}}$CuCl2$\stackrel{FeCl_{3}(aq)}{→}$FeCl2 | |
| C. | FeS2$→_{高温}^{O_{2}}$SO2$\stackrel{H_{2}O_{2}(aq)}{→}$H2SO4 | |
| D. | NH3$→_{催化剂,△}^{O_{2}}$NO2$\stackrel{H_{2}O}{→}$HNO3 |
7.如图为海水综合利用的部分模拟过程.

下列有关说法正确的是( )

下列有关说法正确的是( )
| A. | ①中加人试剂顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液 | |
| B. | 过程②为电解熔融精盐 | |
| C. | 工业上过程③加入的试剂为浓NaOH溶液 | |
| D. | 第④步反应的离子方程式可表示为:2Br-+Cl2=Br2+2Cl- |
5.下列仪器名称正确的是( )
| A. |  三脚架 | B. |  溶量瓶 | C. |  镊子 | D. |  坩锅 |
12.下列反应中,氧元素被还原的是( )
| A. | 2Na+O2$\frac{\underline{\;点燃\;}}{\;}$Na2O2 | B. | Na2O+H2O═2NaOH | ||
| C. | 2F2+2H2O═4HF+O2 | D. | 2C+SiO2$\frac{\underline{\;高温\;}}{\;}$2CO↑+Si |
2.X、Y、Z、W、R 为原子序数依次增大的五种短周期主族元素. X原子的最外层电子数是其内层电子数的2倍,W+与Y2- 具有相同的电子层结构,R 与 Y 可形成RY2、RY3化合物.下列说法正确的是( )
| A. | Y 与氢元素所形成的化合物分子只含有极性键 | |
| B. | W2Y、W2Y2 中阴、阳离子个数比均为 1:2 | |
| C. | Z 的最高价氧化物对应水化物的酸性比 R 的强 | |
| D. | 将XY2通入 W 单质与水反应后的溶液中,生成的盐只有一种 |
9.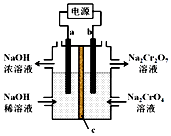 根据反应2CrO42-+2H+?Cr2O72-+H2O 用惰性电极电解Na2CrO4溶液制取Na2Cr2O7,下列说法不正确的是( )
根据反应2CrO42-+2H+?Cr2O72-+H2O 用惰性电极电解Na2CrO4溶液制取Na2Cr2O7,下列说法不正确的是( )
 根据反应2CrO42-+2H+?Cr2O72-+H2O 用惰性电极电解Na2CrO4溶液制取Na2Cr2O7,下列说法不正确的是( )
根据反应2CrO42-+2H+?Cr2O72-+H2O 用惰性电极电解Na2CrO4溶液制取Na2Cr2O7,下列说法不正确的是( )| A. | a连接电源负极 | |
| B. | b极反应式:2H2O-4e-=O2↑+4H+ | |
| C. | c为阳离子交换膜 | |
| D. | 通过2 mol电子时生成1 mol Cr2O72- |
5.常温下,pH=9的CH3COONa溶液和pH=9的NH3•H2O溶液中水的电离程度大小关系是( )
| A. | 前者大 | B. | 后者大 | C. | 一样大 | D. | 无法判断 |
4.下列有关甲烷的取代反应的叙述正确的是( )
| A. | 甲烷与氯气的物质的量之比为1:1,混合发生取代反应只生成CH3C1 | |
| B. | 甲烷与氯气的取代反应,生成的产物中CH3C1最多 | |
| C. | 甲烷与氯气的取代反应生成的产物为混合物 | |
| D. | 1mo1甲烷生成CCl4最多消耗2mo1氯气 |