题目内容
已知酸性: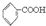 >H2CO3>
>H2CO3> >HCO3-将
>HCO3-将 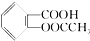 转变为
转变为 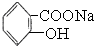 ,可行的方法是( )
,可行的方法是( )
 >H2CO3>
>H2CO3> >HCO3-将
>HCO3-将  转变为
转变为  ,可行的方法是( )
,可行的方法是( )| A、向该溶液中加入足量的稀硫酸,加热 |
| B、将该物质与稀硫酸共热后,再加入足量的NaOH溶液 |
| C、将该物质与足量的NaOH溶液共热,再通入足量CO2气体 |
| D、将该物质与稀硫酸共热后,再加入足量的NaHCO3溶液 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:已知酸性: >H2CO3>
>H2CO3> >HCO3-,将
>HCO3-,将  转变为
转变为  ,则先发生水解反应,然后加入的物质与-COOH反应而不与-OH反应,据此分析.
,则先发生水解反应,然后加入的物质与-COOH反应而不与-OH反应,据此分析.
 >H2CO3>
>H2CO3> >HCO3-,将
>HCO3-,将  转变为
转变为  ,则先发生水解反应,然后加入的物质与-COOH反应而不与-OH反应,据此分析.
,则先发生水解反应,然后加入的物质与-COOH反应而不与-OH反应,据此分析.解答:
解:A. 在酸性条件下水解生成
在酸性条件下水解生成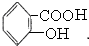 ,故A错误;
,故A错误;
B. 在酸性条件下水解生成
在酸性条件下水解生成 ,再加入足量的NaOH溶液,-COOH和-OH均与NaOH溶液反应,故B错误;
,再加入足量的NaOH溶液,-COOH和-OH均与NaOH溶液反应,故B错误;
C. 与足量的NaOH溶液共热,再通入足量CO2气体,生成
与足量的NaOH溶液共热,再通入足量CO2气体,生成 ,故C正确;
,故C正确;
D. 在酸性条件下水解生成
在酸性条件下水解生成 ,再加入足量的NaHCO3溶液生成
,再加入足量的NaHCO3溶液生成 ,故D正确;
,故D正确;
故选CD.
 在酸性条件下水解生成
在酸性条件下水解生成 ,故A错误;
,故A错误;B.
 在酸性条件下水解生成
在酸性条件下水解生成 ,再加入足量的NaOH溶液,-COOH和-OH均与NaOH溶液反应,故B错误;
,再加入足量的NaOH溶液,-COOH和-OH均与NaOH溶液反应,故B错误;C.
 与足量的NaOH溶液共热,再通入足量CO2气体,生成
与足量的NaOH溶液共热,再通入足量CO2气体,生成 ,故C正确;
,故C正确;D.
 在酸性条件下水解生成
在酸性条件下水解生成 ,再加入足量的NaHCO3溶液生成
,再加入足量的NaHCO3溶液生成 ,故D正确;
,故D正确;故选CD.
点评:本题考查了有机化合物的转化,侧重于官能团的转化的考查,题目难度不大.

练习册系列答案
相关题目
25℃时,下列两溶液混合后所得溶液pH<7的是( )
| A、pH=3的醋酸和pH=11的氢氧化钡溶液等体积混合 |
| B、pH=3的盐酸和pH=11的氨水等体积混合 |
| C、pH=3的盐酸和pH=11的氢氧化钡溶液等体积混合 |
| D、pH=3的硫酸和pH=11的氨水等体积混合 |
下列离子方程式正确的是( )
| A、NH4HCO3溶液中加入少量稀NaOH溶液:NH4++OH-=NH3?H2O |
| B、FeBr2溶液中通入足量的氯气:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
| C、硫酸亚铁溶液中加入用硫酸酸化的双氧水Fe2++2H++H2O2=Fe3++2H2O |
| D、在通入过量SO2后的NaOH溶液中加足量的溴水(不考虑SO2的溶解):HSO3-+Br2+H2O=3H++2Br-+SO42- |
室温下,下列有关两种溶液的说法不正确的是( )
| 序号 | ① | ② |
| pH | 12 | 12 |
| 溶液 | 氨水 | 氢氧化钠溶液 |
| A、①②两溶液中c(OH-)相等 |
| B、①溶液的物质的量浓度为0.01 mol?L-1 |
| C、①②两溶液分别加水稀释10倍,稀释后溶液的pH:①>② |
| D、等体积的①②两溶液分别与0.01 mol?L-1的盐酸完全中和,消耗盐酸的体积:①>② |
常温时,将pH=13的强碱溶液和pH=2的强酸溶液混合,所得溶液的pH=11,则强碱溶液和强酸溶液的体积之比为( )
| A、1:9 | B、9:1 |
| C、10:1 | D、1:10 |
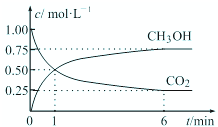 我国政府承诺,到2020年,单位GDP二氧化碳排放量比2005年下降40%~50%.
我国政府承诺,到2020年,单位GDP二氧化碳排放量比2005年下降40%~50%.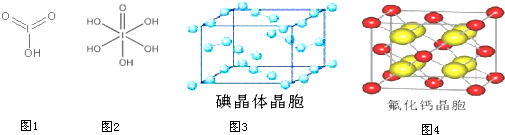
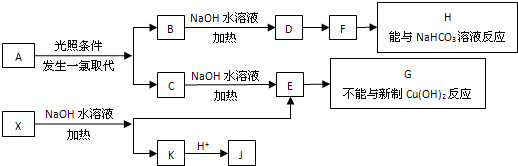
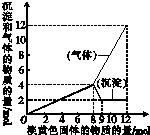 某溶液中可能含有Fe2+、Mg2+、Cu2+、NH4+、Al3+,当加入一种淡黄色固体并加热溶液时,有刺激性气味气体放出和白色沉淀生成;加入淡黄色固体的物质的量(横坐标)与析出沉淀和产生气体的物质的量(纵坐标)的关系如图所示,问所加淡黄色固体是
某溶液中可能含有Fe2+、Mg2+、Cu2+、NH4+、Al3+,当加入一种淡黄色固体并加热溶液时,有刺激性气味气体放出和白色沉淀生成;加入淡黄色固体的物质的量(横坐标)与析出沉淀和产生气体的物质的量(纵坐标)的关系如图所示,问所加淡黄色固体是