题目内容
下列说法正确的是( )
| A、欲粗略测定某未知浓度的醋酸溶液中醋酸的电离常数Ka,应做的实验和所需的试剂(或试纸)为:中和滴定实验、pH试纸 |
| B、在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
| C、C3H2Cl6的六氯代物共有4种,而且CH3-CH=CH-CH3与C3H6一定互为同系物 |
| D、.将0.1 mol/L的NaOH溶液与0.5 mol/L的CuSO4溶液等体积混合制得氢氧化铜悬浊液,用于检验麦芽糖是还原糖 |
考点:弱电解质在水溶液中的电离平衡,有机化合物的异构现象,有机化学反应的综合应用
专题:电离平衡与溶液的pH专题,有机反应
分析:A、确定醋酸的电离常数,根据CH3COOH?CH3COO-+H+,应分别确定CH3COOH的物质的量浓度和H+的物质的量浓度,可用滴定法确定CH3COOH的物质的量浓度,用pH试纸可粗略确定H+的物质的量浓度;
B、羧酸跟醇的反应过程一般是:羧酸分子中的羟基与醇分子中羟基的氢原子结合成水,其余部分互相结合成酯,即酸去羟基醇去羟基氢;
C、6六氯丙烷的同分异构体只有2种;C3H6可能是环丙烷;
D、检验醛基时应在碱性条件下进行;
B、羧酸跟醇的反应过程一般是:羧酸分子中的羟基与醇分子中羟基的氢原子结合成水,其余部分互相结合成酯,即酸去羟基醇去羟基氢;
C、6六氯丙烷的同分异构体只有2种;C3H6可能是环丙烷;
D、检验醛基时应在碱性条件下进行;
解答:
解:A、可用滴定法确定CH3COOH的物质的量浓度,用pH试纸可粗略确定H+的物质的量浓度,进而计算电离常数,故A正确;
B、乙酸与乙醇反应中乙酸提供羟基,醇提供羟基氢原子,结合生成水,其余部分互相结合成酯,由于酯化反应是可逆反应,故18O只存在于乙醇中,故B错误;
C、6六氯丙烷的同分异构体只有2种;C3H6可能是环丙烷,与2-丁烯不是同系物,故C错误;
D、0.1mol/L的氢氧化钠溶液与0.5mol/L的硫酸铜溶液等体积混合,恰好生成氢氧化铜沉淀,检验醛基时应在碱性条件下进行,故应使氢氧化钠稍过量,故D错误;
故选A.
B、乙酸与乙醇反应中乙酸提供羟基,醇提供羟基氢原子,结合生成水,其余部分互相结合成酯,由于酯化反应是可逆反应,故18O只存在于乙醇中,故B错误;
C、6六氯丙烷的同分异构体只有2种;C3H6可能是环丙烷,与2-丁烯不是同系物,故C错误;
D、0.1mol/L的氢氧化钠溶液与0.5mol/L的硫酸铜溶液等体积混合,恰好生成氢氧化铜沉淀,检验醛基时应在碱性条件下进行,故应使氢氧化钠稍过量,故D错误;
故选A.
点评:本题考查了弱酸电离常数的实验测定、酯化反应、同系物和同分异构体、检验醛基的实验,题目难度较大.

练习册系列答案
相关题目
能正确表示下列化学反应的离子方程式是( )
| A、用氢氧化钠溶液吸收少量二氧化硫:2OH-+SO2═SO32-+H2O |
| B、金属铝溶于盐酸中:Al+2H+═Al3++H2↑ |
| C、硫酸铜溶液与氢氧化钡溶液反应:SO42-+Ba2+═BaSO4↓ |
| D、碳酸镁溶于硝酸中:CO32-+2H+═H2O+CO2↑ |
在下列物质 ①NaHCO3 ②MgCl2 ③Na2CO3 ④(NH4)2CO3中,与盐酸和氢氧化钙溶液均可反应的是( )
| A、③④ | B、①③④ | C、② | D、① |
下列气体:①Cl2 ②SO2 ③NO2 ④NH3 ⑤H2S ⑥H2不能用浓硫酸干燥的是( )
| A、只有④ | B、④⑤ |
| C、②④⑤⑥ | D、全部 |
下列关于葡萄糖的说法错误的是( )
| A、葡萄糖的分子式是C6H12O6 |
| B、葡萄糖属于单糖 |
| C、葡萄糖是碳水化合物,因为它的分子是由6个碳原子和6个水分子组成 |
| D、葡萄糖能与新制的氢氧化铜悬浊液共热反应,生成砖红色的沉淀 |
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
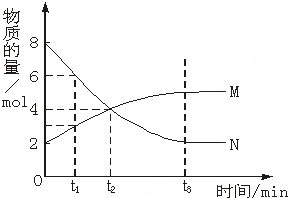

| A、反应的化学方程式为:M?N |
| B、t2时,正逆反应速率相等,达到平衡 |
| C、t3时,正反应速率大于逆反应速率 |
| D、t1时,N的浓度是M浓度的2倍 |
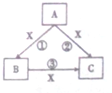 在化学反应中,反应物相同时,因反应条件不同或反应物的量不同产物可能不同,已知A,B,C,X均为中学化学中的常见物质,在常温下它们有如图转化关系(部分产物已略去)回答下列问题
在化学反应中,反应物相同时,因反应条件不同或反应物的量不同产物可能不同,已知A,B,C,X均为中学化学中的常见物质,在常温下它们有如图转化关系(部分产物已略去)回答下列问题