题目内容
(8分)活性氧化锌用作橡胶硫化的活性剂、补强剂。以氧化锌粗品为原料制备活性氧化锌的生产工艺流程如下:

一些阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Cu(OH)2 | Zn(OH)2 | Fe(OH)2 |
pH | 3.2 | 6.7 | 8.0 | 9.7 |
(1)“溶解”后得到的酸性溶液中含有Zn2+、SO42-,另含有Fe2+、Cu2+等杂质。先加入__________(填“Na2CO3”或“H2SO4”)调节溶液的pH至5.4,然后加入适量KMnO4,Fe2+转化为Fe(OH)3,同时KMnO4转化为MnO2。经检测溶液中Fe2+的浓度为0.009 mol·L-1,则每升溶液中至少应加入________mol KMnO4。
(2)杂质Cu2+可利用置换反应除去,应选择的试剂是____________________________。
(3)“沉淀”得到ZnCO3·2Zn(OH)2·H2O,“煅烧”在450~500 ℃下进行,“煅烧”反应的化学方程式为___________________________________________________。
(每空2分,8分)(1)Na2CO3 0.003 (2)锌粉
(3)ZnCO3·2Zn(OH)2·H2O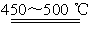 3ZnO+CO2↑+3H2O↑
3ZnO+CO2↑+3H2O↑
【解析】
试题分析:(1)要沉淀金属阳离子,则需要降低溶液的酸性,因此应该加入碳酸钠。1L溶液中亚铁离子的物质的量是0.009mol,在反应中被氧化为铁离子,失去0.009mol电子。高锰酸钾被还原为二氧化锰,锰元素化合价从+7价降低到+4价,得到3个电子,则根据电子得失守恒可知需要高锰酸钾的物质的量是0.009mol÷3=0.003mol。
(2)由于不能引入杂质,则要置换出铜,应该选择锌粉。
(3)ZnCO3·2Zn(OH)2·H2O煅烧时得到氧化锌、CO2和水,反应的化学方程式为ZnCO3·2Zn(OH)2·H2O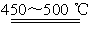 3ZnO+CO2↑+3H2O↑。
3ZnO+CO2↑+3H2O↑。
考点:考查物质制备工艺流程图的分析与应用

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 H++OH- △H>0。下列叙述正确的是
H++OH- △H>0。下列叙述正确的是 HCOO-+ H3O+ B.CO2+H2O
HCOO-+ H3O+ B.CO2+H2O □+2FeS + SO2 (已配平),则下列关于该反应的说法错误的是
□+2FeS + SO2 (已配平),则下列关于该反应的说法错误的是