题目内容
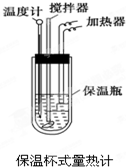 在量热计中(如图)将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.
在量热计中(如图)将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.(1)试求CH3COOH的中和热△H表达数值式.
(2)上述数值结果与57.3kJ/mol有偏差,产生原因可能是
a.实验装置保温、隔热效果差
b.配制0.55mol/L NaOH溶液时俯视刻度线读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
e.用量筒量取NaOH溶液的体积时仰视读数.
考点:中和热的测定
专题:化学反应中的能量变化
分析:(1)根据化学反应热的计算公式Q=-cm△T来计算;
(2)a.实验装置保温、隔热效果必须好;b.配制0.55mol/L NaOH溶液时视线要和凹液面相平;
c.允许分多次把NaOH溶液倒入盛有硫酸的小烧杯中;d.用温度计测定NaOH溶液起始温度后,要将温度计回零直再测定H2SO4溶液的温度;e.量取NaOH溶液的体积时视线要和凹液面相平;
(2)a.实验装置保温、隔热效果必须好;b.配制0.55mol/L NaOH溶液时视线要和凹液面相平;
c.允许分多次把NaOH溶液倒入盛有硫酸的小烧杯中;d.用温度计测定NaOH溶液起始温度后,要将温度计回零直再测定H2SO4溶液的温度;e.量取NaOH溶液的体积时视线要和凹液面相平;
解答:
解:(1)CH3COOH的中和热Q=△H=Q=-cm△T=
=-5.33×104 J?mol-1=-53.3 kJ?mol-1,
答:CH3COOH的中和热△H=-53.3 kJ?mol-1;
(2)a.实验装置保温、隔热效果必须好,否则影响实验结果,故a正确;
b.配制0.55mol/L NaOH溶液时俯视刻度线读数,会导致所量的氢氧化钠浓度偏大,影响实验结果,故b正确;
c.允许分多次把NaOH溶液倒入盛有硫酸的小烧杯中,故c错误;
d.用温度计测定NaOH溶液起始温度后,要将温度计回零直再测定H2SO4溶液的温度,直接测定影响实验结果,故d正确;
e.量取NaOH溶液的体积时仰视读数,会导致所量的氢氧化钠体积偏大,影响实验结果,故e正确;
故答案为:abde;
| [150.5J/K+4.184J?(g?K)-1×200g]×(300.7-298)K |
| 0.05mol |
答:CH3COOH的中和热△H=-53.3 kJ?mol-1;
(2)a.实验装置保温、隔热效果必须好,否则影响实验结果,故a正确;
b.配制0.55mol/L NaOH溶液时俯视刻度线读数,会导致所量的氢氧化钠浓度偏大,影响实验结果,故b正确;
c.允许分多次把NaOH溶液倒入盛有硫酸的小烧杯中,故c错误;
d.用温度计测定NaOH溶液起始温度后,要将温度计回零直再测定H2SO4溶液的温度,直接测定影响实验结果,故d正确;
e.量取NaOH溶液的体积时仰视读数,会导致所量的氢氧化钠体积偏大,影响实验结果,故e正确;
故答案为:abde;
点评:本题考查学生中和热的测定知识,注意稀的强酸和强碱溶液发生中和反应生成1mol水所放出的热量即为中和热.注意测定反应热的误差.

练习册系列答案
相关题目
(1)写出下列官能团的名称:
①-COOH ②-OH
(2)现有4种有机物:①乙烯,②乙醇,③乙酸,④乙酸乙酯(填写结构简式):
能发生水解反应的是
具有酸性且能发生酯化反应的是 .
能发生加成反应的是 .
①-COOH
(2)现有4种有机物:①乙烯,②乙醇,③乙酸,④乙酸乙酯(填写结构简式):
能发生水解反应的是
具有酸性且能发生酯化反应的是
能发生加成反应的是
下列叙述正确的是( )
| A、锥形瓶可用作加热的反应器 |
| B、室温下,不能将浓硫酸盛放在铁桶中 |
| C、pH试纸使用时不能用蒸馏水润湿,如果润湿,测溶液的pH时,结果一定会有偏差 |
| D、配制溶液定容时,俯视容量瓶刻度会使溶液浓度偏高 |

 (1)有甲、乙两容器,甲的容积固定,乙的容积可变.在一定温度下,向甲中通入3molN2和4molH2,反应达到平衡时,生成NH3物质的量为amol.
(1)有甲、乙两容器,甲的容积固定,乙的容积可变.在一定温度下,向甲中通入3molN2和4molH2,反应达到平衡时,生成NH3物质的量为amol. 和一个-Cl,它的可能结构分别是
和一个-Cl,它的可能结构分别是