题目内容
5.工业制硫酸生产流程如图1: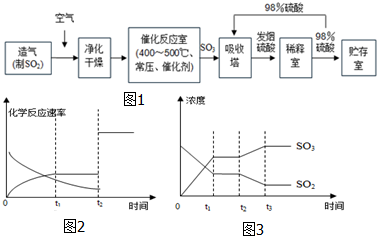
催化室的反应为:2SO2+O2?2SO3△H<0
(1)在沸腾炉中,需要将黄铁矿粉碎的目的是增大固体的接触面积,提高反应速率.
(2)在催化反应室,下列措施中有利于提高SO2平衡转化率的有cd.(填写编号)
a.减少压强 b.升高温度 c.不断补充空气 d.及时分离出SO3
(3)在450℃、常压和钒催化条件下,在容积为VL的恒容容器中加入2n molSO2和n molO2判断反应达到平衡状态的标志是bc.(填写编号)
a.SO2和SO3浓度相等 b.SO2百分含量保持不变
c.容器中气体的压强不变 d.SO3的生成速率与SO2的消耗速率相等
(4)图2、3表示该SO2和O2的反应在时刻t1达到平衡、在时刻t2因改变某个条件而发生变化的情况:
①图2中时刻t2发生改变的条件是催化剂.
②图3中时刻t2发生改变的条件是降低温度.
分析 (1)黄铁矿粉碎会增大反应物的接触面积加快反应速度;
(2)提高SO2平衡转化率,促进化学平衡向右移动,根据化学平衡移动影响因素判断;
(3)根据化学平衡状态特征判断分析,达到平衡时,一是等,二是定:
等是指v正=v逆,同一种物质:该物质的生成速率等于它的消耗速率;不同的物质:速率之比等于方程式中各物质的计量数之比,但必须是不同方向的速率;
定是指各成分含量保持不变:
①各组成成分的质量、物质的量、分子数、体积(气体)、物质的量浓度均保持不变;
②各组成成分的质量分数、物质的量分数、气体的体积分数均保持不变;
③若反应前后的物质都是气体,且总体积不等,则气体的总物质的量、总压强(恒温、恒容)、平均摩尔质量、混合气体的密度(恒温、恒压)均保持不变;
④反应物的转化率、产物的产率保持不变;
(4)根据外界条件对化学平衡的影响判断,图2中t2正逆反应速率同时同等程度增大,对于2SO2+O2?2SO3,使用催化剂才能实现正逆反应速率同时同等程度增大;图3中时刻t2 SO3浓度增大,SO2浓度减小,即化学平衡向右移动,从温度、压强对平衡的影响进行分析.
解答 解:(1)反应物接触面积越大,反应越剧烈,黄铁矿粉碎会增大反应物的接触面积,加快反应速度,故答案为:增大固体的接触面积,提高反应速率;
(2)提高SO2平衡转化率,促进化学平衡向右移动,
a.正反应方向气体体积减小,减小压强,化学平衡向逆反应方向移动,故a错误;
b.正反应方向放热,升高温度,化学平衡向逆反应方向移动,故b错误;
c.增大氧气浓度,化学平衡向右移动,故c正确;
d.减小生成物浓度,化学平衡向右移动,故d正确;
故答案为:cd;
(3)a、SO2和SO3浓度相等,并不能说明各物质浓度不变,不能判断是否平衡,故a错误;
b、SO2百分含量保持不变,即各物质浓度不再发生变化,达到化学平衡状态,故b正确;
c、反应前后气体物质的量不同,容器中气体的压强不变,则达到化学平衡状态,故c正确;
d、SO3的生成速率与SO2的消耗速率相等,均为正反应方向,不能判断正逆反应速率是否相等,不能判断是否平衡,故d错误;
故答案为:bc;
(4)图2中,t2正逆反应速率同时同等程度增大,由于反应前后气体物质的量不同,增大压强化学平衡发生移动,即正逆反应速率变化程度不同,所以外界条件只能为加入催化剂;图3中时刻t2 SO3浓度增大,SO2浓度减小,即化学平衡向右移动,又由于在t2时,二者浓度不变,即压强不变,或者说,不是因为压强变化而导致平衡的移动,只能为温度的影响,所以条件为降低温度,故答案为:加入催化剂;降低温度.
点评 本题是一道综合性的考题,涉及化学反应速率、化学平衡的移动以及v-t图的知识,难度较大,综合性强.

 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案| A. | 3种 | B. | 2种 | C. | 4种 | D. | 无法判断 |

(1)若从下列四个城市中选择一处新建一座硫酸厂,你认为厂址宜选在C的郊区(填标号)
A.有丰富黄铁矿资源的城市 B.风光秀丽的旅游城市
C.消耗硫酸甚多的工业城市 D.人口稠密的文化、商业中心城市
(2)沸腾炉中发生反应的化学方程式为4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$ 2Fe2O3+8SO2,接触室中发生反应的化学方程式是2SO2+O2$?_{△}^{催化剂}$ 2SO3.
(3)在硫酸工业制法中,下列生产操作与说明生产操作的主要原因二者都正确的是D.
A.硫铁矿燃烧前要粉碎,因为大块的黄铁矿不能在空气中反应
B.从沸腾炉出来的气体要净化,因为炉气中的SO2会与杂质反应
C.SO2氧化成SO3要用催化剂,这样可提高SO2的转化率
D.SO3用98.3%的浓硫酸来吸收,目的是为了防止形成酸雾,以提髙SO3吸收效率
(4)表是压强对SO2平衡转化率的影响
| 压强Mpa 转化率% 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
(5)某工厂用500t含硫量为48%的黄铁矿制备硫酸,若在沸腾炉中有2%的FeS2损失,在接触室中SO3的产率为96%,则可得到98%的浓硫酸的质量是376.32tt.
| A. | 该溶液中H+、NH4+、NO3-、Al3+可以大量共存 | |
| B. | 该溶液中通入足量CO2气体无明显现象 | |
| C. | 用该溶液浸泡锅炉中的水垢,可使硫酸钙转化为碳酸钙 | |
| D. | 与苯酚溶液反应的离子方程式为:2C6H5OH+CO32-→2C6H5O-+H2O+CO2↑ |
| A. | 由铝土矿冶铝:铝土矿$→_{Na_{3}AlF_{6}}^{电解}$Al | |
| B. | 制硫酸:硫铁矿$→_{空气}^{高温}$SO2$\stackrel{H_{2}O}{→}$H2SO3$\stackrel{O_{2}}{→}$H2SO4 | |
| C. | 由NaCl制漂白粉:NaCl(aq)$\stackrel{电解}{→}$Cl2$\stackrel{石灰乳}{→}$漂白粉 | |
| D. | 合成氨:NH4Cl和Ca(OH)2固体$\stackrel{△}{→}$NH3$\stackrel{碱石灰}{→}$纯净干燥的氨气 |

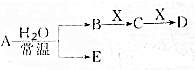 已知A、B、C、D、E、X的转化关系如图所示:
已知A、B、C、D、E、X的转化关系如图所示: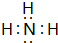 B位于周期表中第二周期ⅦA族.
B位于周期表中第二周期ⅦA族.