题目内容
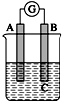 如图所示装置,检流计指针发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的( )
如图所示装置,检流计指针发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的( )| A、A是Zn,B是Cu,C为稀硫酸 |
| B、A是Ag,B是Fe,C为稀AgNO3溶液 |
| C、A是Fe,B是Ag,C为稀AgNO3溶液 |
| D、A是Cu,B是Zn,C为稀硫酸 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:原电池中负极的活泼性大于正极的活泼性,负极上金属失电子变成离子进入溶液,质量减少,正极上得电子发生还原反应,正极上析出物质,若析出的物质是金属,则正极质量增加,据此分析.
解答:
解:该原电池中,A极逐渐变粗,B极逐渐变细,所以B作负极,A作正极,B的活泼性大于A的活泼性,所以排除AC选项;
A极逐渐变粗,说明有金属析出,D选项析出氢气不是金属,B选项析出金属,所以B符合题意.
故选B.
A极逐渐变粗,说明有金属析出,D选项析出氢气不是金属,B选项析出金属,所以B符合题意.
故选B.
点评:本题考查了原电池原理,难度不大,明确正负极的判断方法,注意不能仅根据金属的活泼性判断正负极,要根据发生反应的反应类型判断正负极,如:Mg、Al、NaOH溶液构成的原电池,铝作负极,镁作正极.

练习册系列答案
相关题目
工业上制造玻璃时不需要用到的原料是( )
| A、纯碱石 | B、石灰 | C、石英 | D、食盐 |
用NA表示阿伏加德罗常数的值.下列叙述不正确的是( )
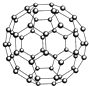

| A、28 g N60单质(见如图)中含有的N-N键键数为3NA |
| B、常温常压下,28 g C2H4和C3H6的混合气体中含有碳原子的数目为2NA |
| C、一定温度下,1 L0.5mol/L 的NH4Cl溶液与2 L 0.25 moL/L NH4Cl溶液含NH4+数目相等 |
| D、含有2NA个阴离子的CaC2在标准状况下,能产生约44.8L的乙炔气体 |
 如图表示反应X(g)+Y(s)?Z(s)+R(g)(△H<0)的正、逆反应速率(v)与时间(t)的关系,t1时开始改变条件,则改变的条件符合曲线的是( )
如图表示反应X(g)+Y(s)?Z(s)+R(g)(△H<0)的正、逆反应速率(v)与时间(t)的关系,t1时开始改变条件,则改变的条件符合曲线的是( )| A、减少物质Z | B、升温 |
| C、减压 | D、用催化剂 |
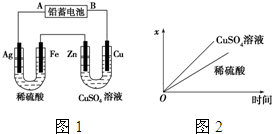 已知铅蓄电池的工作原理为Pb+PbO2+2H2SO2
已知铅蓄电池的工作原理为Pb+PbO2+2H2SO2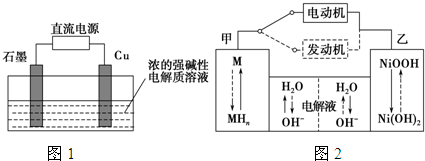
 科学家最近在-100℃的低温下合成一种烃X,此分子的模型如图(图中的连线表示化学键).
科学家最近在-100℃的低温下合成一种烃X,此分子的模型如图(图中的连线表示化学键).