题目内容
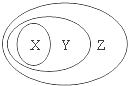 用如图表示的一些物质或概念间的从属关系中不正确的是( )
用如图表示的一些物质或概念间的从属关系中不正确的是( )| X | Y | Z | |
| A | 氧化物 | 化合物 | 纯净物 |
| B | 盐 | 离子化合物 | 化合物 |
| C | 胶体 | 分散系 | 混合物 |
| D | 碱性氧化物 | 金属氧化物 | 氧化物 |
| A、A | B、B | C、C | D、D |
考点:酸、碱、盐、氧化物的概念及其相互联系,混合物和纯净物,单质和化合物,分散系、胶体与溶液的概念及关系
专题:物质的分类专题
分析:由图可知,概念的范畴为Z包含Y,Y包含X,然后利用物质的组成和性质来分析物质的类别,再根据概念的从属关系来解答.
解答:
解:A.氧化物属于化合物,化合物又属于纯净物,故A正确;
B.离子化合物和盐都属于化合物,但某些共价化合物是盐,入AlCl3是共价化合物,则化合物包含离子化合物,离子化合物不一定包含盐,故B错误;
C.胶体属于分散系,而分散系都是由两种以上的物质组成,则属于混合物,故C正确;
D.氧化物只有两种元素组成,则碱性氧化物与金属氧化物都属于氧化物,碱性氧化物都是由金属元素和氧元素组成,但金属氧化物不一定是碱性氧化物,如过氧化钠等,则金属氧化物包含碱性氧化物,故D正确.
故选B.
B.离子化合物和盐都属于化合物,但某些共价化合物是盐,入AlCl3是共价化合物,则化合物包含离子化合物,离子化合物不一定包含盐,故B错误;
C.胶体属于分散系,而分散系都是由两种以上的物质组成,则属于混合物,故C正确;
D.氧化物只有两种元素组成,则碱性氧化物与金属氧化物都属于氧化物,碱性氧化物都是由金属元素和氧元素组成,但金属氧化物不一定是碱性氧化物,如过氧化钠等,则金属氧化物包含碱性氧化物,故D正确.
故选B.
点评:本题考查物质的组成和分类,比较简单,属于基础题.学生应能识别常见物质的种类,并能利用其组成来判断物质的类别是解答的关键.

练习册系列答案
相关题目
氯化硼(BCl3)的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,它能水解,有关叙述正确的是( )
| A、氯化硼液态时能导电而固态时不导电 |
| B、氯化硼加到水中使溶液的pH升高 |
| C、氯化硼分子呈平面正三角形,属非极性分子 |
| D、氯化硼B-Cl之间是sp3形成的σ键 |
某离子反应涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒.其中c(NH4+)随反应进行逐渐减小.下列判断错误的是( )
| A、反应的氧化剂是ClO- |
| B、消耗1mol还原剂,转移电子3mol |
| C、氧化剂与还原剂的物质的量之比为2:3 |
| D、反应后溶液的酸性明显增强 |
运用元素周期律分析以下推断,其中不正确的是( )
| A、已知Ra是第七周期、ⅡA族的元素,故Ra(OH)2的碱性比Mg(OH)2的碱性强 |
| B、已知As是第四周期、ⅤA族的元素,故AsH3的稳定性比NH3的稳定性强 |
| C、已知Cs的原子半径比Na的原子半径大,故Cs与水反应比Na与水反应更剧烈 |
| D、已知Cl的核电荷数比Al的核电荷数大,故Cl的原子半径比Al的原子半径小 |
 用惰性电极电解NaHSO3溶液可以得到硫酸,装置如图所示.电解过程中①、②、③、④处的生成物依次是( )
用惰性电极电解NaHSO3溶液可以得到硫酸,装置如图所示.电解过程中①、②、③、④处的生成物依次是( )| A、硫酸、氧气和二氧化硫、氢气、亚硫酸钠 |
| B、硫酸、氢气、氧气和二氧化硫、亚硫酸钠 |
| C、亚硫酸钠、氧气和二氧化硫、氢气、硫酸 |
| D、亚硫酸钠、氢气、氧气和二氧化硫、硫酸 |
下列反应最能体现“原子经济”的是( )
| A、甲烷与氯气制备一氯甲烷 |
| B、乙烯聚合为聚乙烯高分子材料 |
| C、以铜和浓硝酸为原料生产硝酸铜 |
| D、用苯和浓硝酸反应制取硝基苯 |
下列离子方程式正确的是( )
| A、把Fe(OH)3放入氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O | ||||
B、Mg (HCO3)2溶液和足量的澄清石灰水反应:Mg2++2HCO
| ||||
C、Ca(HCO3)2溶液和过量NaOH溶液反应:Ca2++2HCO
| ||||
| D、把Mg粉放入FeCl3溶液中:2Fe3++3Mg+6H2O=2Fe(OH)3↓+3Mg2++3H2↑ |