题目内容
标准状况下 VL NH3溶于1L的水中形成密度为ρg/cm3的氨水,求该氨水的物质的量浓度: .
考点:物质的量浓度的相关计算
专题:计算题
分析:1L水的质量约为1000g,根据n=
计算出氨气的物质的量,再根据m=nM计算出其质量,从而得出溶液的质量,再根据V=
计算出该溶液体积,最后根据c=
计算出所带溶液的物质的量浓度.
| V |
| Vm |
| m |
| ρ |
| n |
| V |
解答:
解:标准状况下VL NH3的物质的量为:
=
mol,该氨气的质量为:17g/mol×
mol=
g,
1L水的质量约为1000g,则所带溶液的质量为:1000g+
g=(1000+
)g,
所带溶液的体积为:V=
=
mL=
L,
该氨水的物质的量浓度为:c=
=
mol/L,
故答案为:
mol/L.
| VL |
| 22.4L/mol |
| V |
| 22.4 |
| V |
| 22.4 |
| 17V |
| 22.4 |
1L水的质量约为1000g,则所带溶液的质量为:1000g+
| 17V |
| 22.4 |
| 17V |
| 22.4 |
所带溶液的体积为:V=
(1000+
| ||
| ρg/cm3 |
| 22400+17V |
| 22.4ρ |
| 22400+17V |
| 22400ρ |
该氨水的物质的量浓度为:c=
| ||
|
| 1000Vρ |
| 22400+17V |
故答案为:
| 1000Vρ |
| 22400+17V |
点评:本题考查了物质的量浓度的计算,题目浓度中等,正确计算溶液体积为解答关键,注意掌握物质的量浓度的概念及计算方法,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
下列各物质中,互为同系物的是( )
| A、乙醇和乙二醇 |
| B、甲苯和二甲苯 |
| C、溴苯和对二溴苯 |
| D、戊烷和2,2-二甲基丙烷 |
下列粒子的电子式正确的是( )
A、-OH 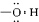 |
B、-OH 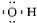 ? ? |
C、-OH 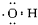 |
D、OH- 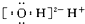 |
A、B、C为短周期非金属元素,其相关性质如下:下列叙述正确的是( )
| 元素 | X | Y | Z |
| 与H2反应条件 | 暗处反应 | 光照 | 高温、催化剂 |
| 常温下氢化物水溶液的pH | 小于7 | 小于7 | 大于7 |
| A、非金属性X<Y |
| B、最外层电子数Z>Y |
| C、Z为第VA族元素 |
| D、Y、Z的氢化物反应形成离子化合物 |
根据下列物质的名称,就能确认是纯净物的是( )
| A、二甲苯 | B、三溴乙烷 |
| C、二氯甲烷 | D、己烯 |
用下列方法制得相同质量的氧气,下列四种方法中所转移的电子数目之比是 ( )
①KMnO4受热分解 ②KClO3受热分解(用MnO2作催化剂)③2H2O2
2H2O+O2↑ ④2Na2O2+2H2O═4NaOH+O2↑.
①KMnO4受热分解 ②KClO3受热分解(用MnO2作催化剂)③2H2O2
| ||
| A、3:2:1:4 |
| B、1:1:1:1 |
| C、1:2:1:2 |
| D、2:2:1:1 |
设NA表示阿伏伽德罗常数,下列说法中正确的是( )
| A、NA个N2分子和NA个CO分子质量比为13:14 |
| B、1molH2O的质量等于NA个H2O质量的总和 |
| C、在任何条件下1molH2所含的原子数为NA |
| D、1molH2SO4中所含的离子数目一定是NA |
下列各项所述的数字中与其他三项不相同的一项是( )
| A、H2O分子的价电子总数 |
| B、在NaCl晶体中,与一个Na+最近的且距离相等的Cl-的个数 |
| C、金属钠的晶胞中钠原子的配位数 |
| D、氯化铯晶体中Cs+的配位数 |