题目内容
3.实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应方程式如下:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O反应中氧化剂是KMnO4,氧化产物是Cl2;当有lmol电子发生转移时,生成氯气的体积(标准状况)11.2L.分析 2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中,Mn元素的化合价降低,Cl元素的化合价升高,以此来解答.
解答 解:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中,Mn元素的化合价降低,Cl元素的化合价升高,则化剂是KMnO4,Cl失去电子被氧化,则氧化产物是Cl2,生成5mol氯气转移10mol电子,则当有lmol电子发生转移时,生成氯气的体积(标准状况)1mol×$\frac{5}{10}$×22.4L/mol=11.2L,
故答案为:KMnO4;Cl2;11.2L.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意电子转移计算,题目难度不大.

练习册系列答案
相关题目
13.下列过程没有发生化学反应的是( )
| A. | 用浸泡过高锰酸钾溶液的硅藻土保鲜水果 | |
| B. | 用热碱水清除炊具上残留的油污 | |
| C. | 用活性炭去除冰箱中的异味 | |
| D. | 用含硅胶、铁粉的透气小袋与食品一起密封包装 |
8.下列说法中,不正确的是( )
| A. | 维勒用无机物合成了尿素,突破了无机物与有机物的界限 | |
| B. | 开发核能、太阳能等新能源,推广乙醇汽油,使用无磷洗涤剂都可直接降低碳排放量 | |
| C. | 红外光谱仪、核磁共振仪、质谱仪都可用于有机化合物结构的分析 | |
| D. | 甲烷是重要的化工原料,其分解产物可用于合成氨和橡胶工业 |
12.硫酸铜是一种应用极其广泛的化工原料.以下是某工厂用含铁废铜为原料生产胆矾(CuSO4•5H2O)的生产流程示意图:

胆矾和石膏在不同温度下的溶解度(g/100g水)见表.
请回答下列问题:
(1)红棕色滤渣的主要成分是Fe(OH)3;
(2)写出浸出过程中生成硫酸铜的化学方程式3Cu+2HNO3+3H2SO4=3CuSO4+2NO↑+4H2O;
(3)操作I的操作温度应该控制在100℃左右;
(4)从溶液中分离出硫酸铜晶体的操作II应为冷却结晶、过滤 洗涤、干燥;
(5)反应产物中的NO可以循环使用,试仅用一个化学方程式表示NO转化为HNO3:4NO+3O2+H2O=4HNO3.

胆矾和石膏在不同温度下的溶解度(g/100g水)见表.
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
(1)红棕色滤渣的主要成分是Fe(OH)3;
(2)写出浸出过程中生成硫酸铜的化学方程式3Cu+2HNO3+3H2SO4=3CuSO4+2NO↑+4H2O;
(3)操作I的操作温度应该控制在100℃左右;
(4)从溶液中分离出硫酸铜晶体的操作II应为冷却结晶、过滤 洗涤、干燥;
(5)反应产物中的NO可以循环使用,试仅用一个化学方程式表示NO转化为HNO3:4NO+3O2+H2O=4HNO3.
13.下列物质中不属于离子晶体的是( )
| A. | 氯化铵 | B. | 硫酸 | C. | 食盐 | D. | 氧化钠 |
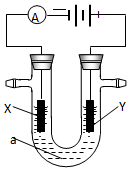 ( 1 )工业上通过电解饱和氯化钠溶液的方法获得氢氧化钠,我国的氯碱工业大多采用离子交换膜电解槽.写出电解饱和氯化钠溶液时的电极反应和总的离子反应方程式:
( 1 )工业上通过电解饱和氯化钠溶液的方法获得氢氧化钠,我国的氯碱工业大多采用离子交换膜电解槽.写出电解饱和氯化钠溶液时的电极反应和总的离子反应方程式: 如图是硫酸试剂瓶标签上的内容:
如图是硫酸试剂瓶标签上的内容: