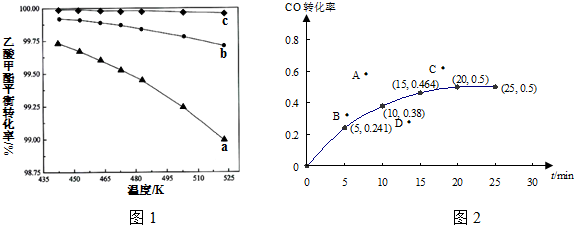
��Ŀ����
4��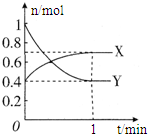 ��һ���¶��£����Ϊ2L���ܱ������У�NO2��N2O4֮�䷢����Ӧ��
��һ���¶��£����Ϊ2L���ܱ������У�NO2��N2O4֮�䷢����Ӧ��2NO2 ��g�� ������ɫ��?N2O4��g�� ����ɫ������ͼ��ʾ��
��1���������¶ȣ���v�������ӿ죬v���棩�ӿ죮����ӿ족����������
��2����������Ӧ�ڼס���������ͬ������ͬʱ���У��ֱ��ü���v��NO2��=18mol/��L•min��������v��N2O4��=0.2mol/��L•s���������з�Ӧ���죮
��3����0��1min������X��ʾ�÷�Ӧ��������0.15mol/��Lmin�����÷�Ӧ����ʱ��Y��ת����60%����Ӧ��ʼʱ�뷴Ӧ��ƽ��״̬ʱ��ѹǿ֮��Ϊ14��11��
��4������������֤���÷�Ӧ�Ѵﵽ��ѧƽ��״̬����AB
A��������ѹǿ���ٷ����仯
B��NO2������������ٷ����仯
C������������ԭ���������ٷ����仯
D����ͬʱ��������n mol N2O4��ͬʱ����2n mol NO2
E����Ӧ��ϵ��NO2��N2O4�������Ϊ1��2
��5������ʼʱ����NO2����0.200mol����ﵽƽ��ʱNO2�����ת����Ϊa��������������ʱ�����д�ʩ�����NO2ת���ʵ���A ������ĸ����
A�������¶�
B����СNO2��Ũ��
C�������¶�
D���ٳ���һ������He��
���� ��1�������¶ȣ���v��������v���棩���ӿ죻
��2�����ݷ�Ӧ����֮�ȵ��ڻ�ѧ������֮�ȱȽϣ�
��3������v=$\frac{��c}{��t}$���㷴Ӧ���ʣ����ͼ����������������
��4�����淴Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ���Ӧ�����и����ʵ����ʵ������䡢���ʵ���Ũ�Ȳ����Լ��ɴ������һϵ�����������䣬�ݴ˷������
��5�������NO2ת���ʵ��Ǵ�ʩ����ƽ�������ƶ����ɣ�
��� �⣺��1���������¶ȣ���v��������v���棩���ӿ죬�ʴ�Ϊ���ӿ죻�ӿ죻
��2������v��NO2��=18mol/��L•min��������v ��N2O4��=0.2mol•L-1•min-1��v��NO2��=2v��N2O4��=0.4mol•L-1•s-1=24mol/��L•min�������ҷ�Ӧ�Ͽ죬
�ʴ�Ϊ���ң�
��3��v��X��=$\frac{\frac{0.7mol-0.4mol}{2L}}{1min}$=0.15mol•��L•min��-1��
�÷�Ӧ�������ʱ��Y��ת����Ϊ��$\frac{1mol-0.4mol}{1mol}$=60%��
��ʼʱ��n��X��+n��Y��=0.4mol+1mol=1.4mol��
ƽ��ʱ��n��X��+n��Y��=0.7mol+0.4mol=1.1mol��
����ͬ�����£������ѹǿ֮�ȵ������ʵ���֮�ȣ�
��Ӧ��ʼʱ�뷴Ӧ��ƽ��״̬ʱ��ѹǿ֮��Ϊ1.4mol��1.1mol=14��11��
�ʴ�Ϊ��0.1mol•��L•min��-1��60%��14��11��
��4��A����Ӧǰ������ϵ���Ͳ��ȣ�������ѹǿ���ٷ����仯��֤���ﵽ��ƽ�⣬��A��ȷ��
B��NO2������������ٷ����仯��ƽ���������֤���ﵽ��ƽ�⣬��B��ȷ��
C����Ӧ���е��κ�ʱ�̣�����������ԭ�����������ᷢ���仯����C����
D����ͬʱ��������n mol N2O4��ͬʱ����2n mol NO2������˵�����淴Ӧ������ȣ���D����
E����Ӧ��ϵ��NO2��N2O4�������Ϊ1��2������˵�����淴Ӧ������ȣ���E����
��ѡAB��
��5�������NO2ת���ʵ��Ǵ�ʩ����ƽ�������ƶ����ɣ�
A�������¶�����ƽ�������ƶ����NO2ת���ʣ���A��ȷ��
B����СNO2��Ũ����ƽ�������ƶ���������NO2ת���ʣ���B����
C�������¶�ƽ�������ƶ���������NO2ת���ʣ���C����
D���ٳ���һ������He��ƽ�ⲻ����ת���ʲ��䣬��D����
��ѡA��
���� ���⿼���Ϊ�ۺϣ���Ŀ�Ѷ��еȣ�ע����ջ�ѧ��Ӧ�����Լ���ѧƽ��Ļ���֪ʶ���ɽ����⣮

 ijͬѧ�������ʵ���Ũ��Ϊ0.100 0mol•L-1������ⶨδ֪���ʵ���Ũ�ȵ�����������Һ��ѡ���̪��ָʾ��������д���пհף�
ijͬѧ�������ʵ���Ũ��Ϊ0.100 0mol•L-1������ⶨδ֪���ʵ���Ũ�ȵ�����������Һ��ѡ���̪��ָʾ��������д���пհף���1���ñ�������ζ����������������Һʱ�����ְ�����ʽ�ζ��ܵĻ���������ҡ����ƿ��ֱ�������һ�����ᣬ��Һ�ɺ�ɫ��Ϊ��ɫ������Ӳ��ٱ�ɫ������ֹͣ�ζ���
��2�����в����п���ʹ��������������Һ��Ũ����ֵƫ�͵���DE������ţ���
A����ʽ�ζ���δ�ñ�������ϴ��ֱ��ע�������
B���ζ�ǰʢ������������Һ����ƿ������ˮϴ����û�и���
C����ʽ�ζ����ڵζ�ǰ�����ݣ��ζ���������ʧ
D����ȡ�������ʱ����ʼ���Ӷ������ζ�����ʱ���Ӷ���
E���ζ������У���ƿ�����ڼ��ң�ʹ������Һ����
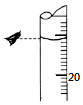
��3����ij�εζ�����ʱ����ʽ�ζ����е�Һ����ͼ��ʾ�������Ϊ10.20 mL�������ӣ���ʹ����ƫ�����С������
��4���ٽ�ϱ����ݣ����㱻������������Һ�����ʵ���Ũ����0.1710 mol•L-1��
| �ζ� ���� | ������Һ ���/mL | ������� | |
| �ζ�ǰ�Ŀ̶�/mL | �ζ���Ŀ̶�/mL | ||
| ��һ�� | 10.00 | 1.34 | 19.39 |
| �ڶ��� | 10.00 | 4.10 | 21.10 |
| ������ | 10.00 | 0.40 | 17.60 |
| A�� | ��ɢ�����ӵĴ�С | B�� | ��ɢ�������Ƿ����� | ||
| C�� | �ܷ������������ | D�� | ��Һ����Ƿ��һ |
| A�� | ͨ��ϡ������ʹѹǿ����ƽ�⽫�����ƶ� | |
| B�� | X������Ӧ������Y ���淴Ӧ���ʵ�$\frac{m}{n}$�� | |
| C�� | �����¶ȣ���������ƽ����Է���������С | |
| D�� | ����X�����ʵ�����ƽ�ⳣ������ |
| A�� | Ԫ��X�ֱ���Y��Z��R�����γɶ��ֶ�Ԫ���ۻ����� | |
| B�� | Ԫ��Y��Z��R�γɵĻ������ˮ��Һ���ܳ����ԡ����Ի������� | |
| C�� | ���ȶ��ԣ�XmYǿ��XmR���е㣺XmY����XmR | |
| D�� | ����Ԫ�صĵ����ڳ���������������̬�������ǹ�̬��һ����Һ̬ |
| A�� | ��������ƽ��ȡ11.72gʳ�� | |
| B�� | ��100mL����Ͳ��ȡ25.00mL���� | |
| C�� | ��pH��ֽ���ij��ˮ��pHΪ4 | |
| D�� | ��0.2000 mol/L����ζ�20.00mLδ֪Ũ��NaOH����ȥ22.40mL������Һ |