题目内容
具有下列电子层结构的原子和离子,其对应元素一定属于同一周期的是
A.两原子核外全部都是s电子
B.最外层电子排布为2s22p6的原子和最外层电子排布为2s22p6的离子
C.原子核外M层上的s、p能级都充满电子,而d能级上没有电子的两种原子
D.两原子N层上都有1个s电子,一个原子有d电子,另一个原子无d电子
D
【解析】
试题分析:A、两原子核外全部都是s电子,不一定是同一周期,如H与Li+,错误;B、最外层电子排布为2s22p6的原子是Ne,最外层电子排布为2s22p6的离子可能是Na、Mg、Al或F的离子,前三种与Ne不是同一周期,错误;C、原子核外M层上的s、p能级都充满电子,而d能级上没有电子的两种原子不一定是同周期,M层上的s、p能级都充满电子,但未说明4s能级上有无电子,所以不能确定是同周期,错误;D、N层上都有1个电子,说明最外层是4s,一个有d电子,一个无d电子,只是说明3d轨道上有无电子,但不影响电子层数,所以都是第四周期元素,正确,答案选D。
考点:考查原子结构域元素位置的关系

练习册系列答案
相关题目
 CO2
CO2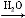 H2CO3
H2CO3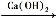 CaCO3
CaCO3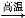 CO2
CO2 Fe3O4 B.C+ O2
Fe3O4 B.C+ O2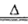 2CO
2CO