题目内容
10.有饱和一元羧酸和饱和一元醇形成的酯A.已知:
①2.2gA燃烧可生成4.4gCO2和1.8gH2O;
②1.76gA与50mL0.5mol/L的NaOH溶液共热后,为了中和剩余的碱液,耗去0.2mol/L的盐酸25mL;
③取A水解后所得的醇0.64g,跟足量的钠反应时,标准状况下收集到224mLH2.经分析求:
(1)A的相对分子质量为:88,分子式为C4H8O2,结构简式为:CH3CH2COOCH3.
(2)写出A与NaOH共热反应的化学方程式:CH3CH2COOCH3+NaOH$\stackrel{△}{→}$CH3CH2COONa+CH3OH.
分析 饱和一元羧酸和饱和一元醇形成的酯A,则A的组成通式为CnH2nO2,计算燃烧生成二氧化碳、水的物质的量,根据C、H原子守恒计算n的值,可以确定A的分子式,水解得到的醇组成通式为CmH2m+1OH,根据生成氢气的体积计算确定醇的组成,进而确定A的组成.
解答 解:(1)饱和一元羧酸和饱和一元醇形成的酯A,则A的组成通式为CnH2nO2,
燃烧生成二氧化碳为$\frac{4.4g}{44g/mol}$=0.1mol,生成水的物质的量为$\frac{1.8g}{18g/mol}$=0.1mol,
则$\frac{2.2}{14n+32}$×n=0.1,解得n=4,
故A的分子式为C4H8O2,相对分子质量为14×4+32=88,
水解得到的醇组成通式为CmH2m+1OH,则$\frac{0.64}{14m+18}$=$\frac{0.224}{22.4}$×2,解得m=1,故醇为CH3OH,
则酸为CH3CH2COOH,可推知A的结构简式为CH3CH2COOCH3,
故答案为:88;C4H8O2;CH3CH2COOCH3;
(2)A与氢氧化钠共热反应方程式为:CH3CH2COOCH3+NaOH$\stackrel{△}{→}$CH3CH2COONa+CH3OH,
故答案为:CH3CH2COOCH3+NaOH$\stackrel{△}{→}$CH3CH2COONa+CH3OH.
点评 本题考查有机物分子式与结构的确定,侧重考查学生分析计算能力,注意充分利用组成通式进行解答.

练习册系列答案
相关题目
3.某烃的分子式为C10H14,不能使溴水褪色,但可使酸性高锰酸钾溶液褪色,分子结构中只含有一个烷基,则此烷基的结构共有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
1.下列说法正确的是( )
| A. | 合成硫酸的工业尾气可以直接排入大气 | |
| B. | 进入接触室的气体,必须先经净化、干燥 | |
| C. | 从沸腾炉中排出的炉渣可以作为肥料 | |
| D. | 在高温、高压下由SO2和O2合成SO3 |
18.下列实验装置能达到实验目的是( )
| A | B | C | D | |
| 实验装置 |  | 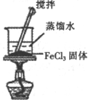 | 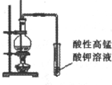 |  |
| 实验目的 | 比较非金属性强弱S>C>Si | 制取少量的Fe(OH)3胶体 | 证明乙醇与浓H2SO4共热生成了乙烯 | 比较不同催化剂的催化效果 |
| A. | A | B. | B | C. | C | D. | D |
15.某中性有机物(分子式为C10H20O2)在稀硫酸作用下加热得到M和N两种有机物,且M被酸性KMnO4溶液作用可直接得到N.下列说法正确的是( )
| A. | M的分子式为C5H10O | |
| B. | 该中性有机物有4种(不考虑立体异构) | |
| C. | 上述过程发生的所有反应与油脂化反应的反应类型相同 | |
| D. | M和N都可以发生取代反应、都能与Na反应生成H2,因此具有相同官能团 |
2.表是元素周期表的一部分,X、Y、Z、W均为短周期元素,X、Z的质子数之和为21.下列说法正确的是( )
| X | Y | ||
| Z | W |
| A. | X元素不能形成氧化物 | |
| B. | Y元素的最高价氧化物的水化物是含氧酸中酸性最强的 | |
| C. | X元素的非金属性比Y元素非金属性强 | |
| D. | 四种元素中,原子半径最小的元素是Y |
19.已知钍${\;}_{90}^{232}$Th的原子可发生下列放射性变化:${\;}_{90}^{232}$Th→${\;}_{88}^{228}$X+${\;}_{2}^{4}$He,生成的X是与Mg同主族的一种元素的原子,下列对X的推断错误的是( )
| A. | X的氢氧化物是一种强碱 | B. | X元素位于第六周期 | ||
| C. | X的碳酸盐难溶于水 | D. | X的最高化合价为+2价 |
20.某元素的离子的结构示意图与Mg2+相同,则下列说法正确的是( )
| A. | 该元素一定在第三周期 | |
| B. | 该元素一定在第二周期 | |
| C. | 若该离子是阳离子,则该元素一定在第三周期 | |
| D. | 若该离子是阴离子,则该元素一定在第三周期 |
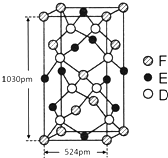 已知A、B、C、D四种短周期元素,它们的核电荷数依次增大.A与C原子的基态电子排布中L能层都有两个未成对电子,C、D同主族. E、F都是第四周期元素,E原子的基态电子排布中有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满.根据以上信息填空:
已知A、B、C、D四种短周期元素,它们的核电荷数依次增大.A与C原子的基态电子排布中L能层都有两个未成对电子,C、D同主族. E、F都是第四周期元素,E原子的基态电子排布中有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满.根据以上信息填空: ,F原子的电子排布式是1s22s22p63s23p63d104s1.
,F原子的电子排布式是1s22s22p63s23p63d104s1. .DAB-的水溶液可以用于实验室中E3+离子的定性检验,形成配合物的颜色为血红色.
.DAB-的水溶液可以用于实验室中E3+离子的定性检验,形成配合物的颜色为血红色.