题目内容
16.(1)同温同压下,容积相同的A、B两容器中分别充满Cl2和SO2,则A、B两容器中Cl2和SO2的物质的量之比是1:1,质量比是71:64.(2)同温同压下,相同质量CO2和CO,分别充入A、B两容器中,气体的物质的量之比是11:7,A、B两容器的体积比是11:7.
分析 (1)同温同压下,容积相同的A、B两容器中分别充满Cl2和SO2,则两种气体的物质的量相等,质量之比等于摩尔质量之比;
(2)根据n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$结合物质的构成计算该题.
解答 解:(1)同温同压下,容积相同的A、B两容器中分别充满Cl2和SO2,则两种气体的物质的量相等,质量之比等于摩尔质量之比,所以A、B两容器中Cl2和SO2的物质的量之比是1:1,质量之比为:35.5×2:64=71:64,故答案为:1:1;71:64;
(2)相同质量的CO2和CO,物质的量之比为$\frac{m}{44}:\frac{m}{28}$=7:11,同温同压下,气体体积之比等于物质的量之比,则CO2和CO体积之比为11:7,
故答案为:11:7;11:7.
点评 本题考查阿伏伽德罗定律及其推论,为高频考点,明确各个物理量之间关系是解本题关键,题目难度不大.

练习册系列答案
相关题目
6.以下属于取代反应的是( )
| A. | 乙烯与溴水的反应 | B. | 甲烷与氯气的反应 | ||
| C. | 乙醇与乙酸的反应 | D. | 苯的燃烧 |
11.下列电子式书写正确的是( )
| A. | 氯化钠 | B. | 氨气 | C. | NH4Cl的电子式  | D. | 硫化钠 |
8.下列实验操作正确的是( )
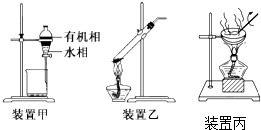

| A. | 用玻璃棒蘸取CH3COOH溶液点在水湿润的pH试纸上,测定该溶液的pH | |
| B. | 用装置甲分液,放出水相后再从分液漏斗上口放出有机相 | |
| C. | 用装置乙加热分解NaHCO3固体 | |
| D. | 用装置丙加热硫酸铜溶液获得CuSO45H2O |
