题目内容
 废铁屑(含铁锈)可用于地下水脱氮,某课题小组模拟地下水脱氮过程,并研究脱氮原理及脱氮效果.
废铁屑(含铁锈)可用于地下水脱氮,某课题小组模拟地下水脱氮过程,并研究脱氮原理及脱氮效果.(1)原料预处理
①先用稀硫酸洗涤废铁屑,其目的是(用离子方程式表示)
(2)脱氮原理的研究
如图表示足量铁屑还原上述KNO3溶液过程中,测出的溶液中相关离子浓度、pH随时间的变化关系(部分副反应产物曲线略去).请根据图中信息回答:
①t1时刻前该反应的离子方程式:
②t1时刻后,该反应仍在进行,溶液中NH4+的浓度在增大,Fe2+的浓度却没有增大,可能的原因是
(3)脱氮效果的研究
①将铁屑和活性炭同时加入上述KNO3溶液中,可以提高脱氮效果,其原因是
②正常地下水中含有CO32-,会影响脱氮的效果,结合文字和化学用语回答其原因(答两点)
考点:含氮物质的综合应用,铁的化学性质
专题:氮族元素
分析:(1)铁的氧化物可以和强酸之间反应,为防止氧气对物质的氧化作用,可以用氮气作保护气;
(2)根据图示知道t1时刻前,硝酸根离子、氢离子浓度逐渐减小,亚铁离子浓度增大,则是金属铁和硝酸之间的反应;亚铁离子属于弱碱阳离子,会发生水解反应;
(3)根据原电池可以加快化学反应速率来回答;
(4)根据实验原理:在酸性环境下,金属铁的脱氮效果更加,结合碳酸根离子水解显碱性来回答.
(2)根据图示知道t1时刻前,硝酸根离子、氢离子浓度逐渐减小,亚铁离子浓度增大,则是金属铁和硝酸之间的反应;亚铁离子属于弱碱阳离子,会发生水解反应;
(3)根据原电池可以加快化学反应速率来回答;
(4)根据实验原理:在酸性环境下,金属铁的脱氮效果更加,结合碳酸根离子水解显碱性来回答.
解答:
解:(1)①铁的表面的铁锈氧化铁可以和稀硫酸之间反应:Fe2O3+6H+=2Fe3++3H2O,为防止氧气对物质的氧化作用,可以用氮气作保护气,应向KNO3溶液中通入氮气,
故答案为:Fe2O3+6H+=2Fe3++3H2O;N2;
(2)①根据图示知道t1时刻前,硝酸根离子、氢离子浓度逐渐减小,亚铁离子浓度增大,则是金属铁和硝酸之间的反应,即4Fe+NO3-+10H+=4Fe2++NH4++3H2O,
故答案为:4Fe+NO3-+10H+=4Fe2++NH4++3H2O;
②根据反应:4Fe+NO3-+10H+=4Fe2++NH4++3H2O,溶液中NH4+的浓度在增大,Fe2+的浓度却没有增大,原因是生成的Fe2+水解所致,故答案为:生成的Fe2+水解;
(3)①将铁屑和活性炭同时加入上述KNO3溶液中,活性炭和铁构成了无数个微小的铁碳原电池加快反应速率(或活性炭吸附作用,降低溶液中NH4+浓度),可以提高脱氮效果,故答案为:活性炭和铁构成了无数个微小的铁碳原电池加快反应速率(或活性炭吸附作用,降低溶液中NH4+浓度);
②根据实验原理:4Fe+NO3-+10H+=4Fe2++NH4++3H2O,在酸性环境下,金属铁的脱氮效果更加,但是CO32-+H2O?HCO3-+OH-,增大了溶液的pH会降低脱氮效果,并且Fe2++CO32-=FeCO3↓,这样碳酸亚铁沉淀覆盖在反应物的表面阻止反应进行,
故答案为:CO32-+H2O?HCO3-+OH-,增大了溶液的pH会降低脱氮效果,且Fe2++CO32-=FeCO3↓,覆盖在反应物的表面阻止反应进行.
故答案为:Fe2O3+6H+=2Fe3++3H2O;N2;
(2)①根据图示知道t1时刻前,硝酸根离子、氢离子浓度逐渐减小,亚铁离子浓度增大,则是金属铁和硝酸之间的反应,即4Fe+NO3-+10H+=4Fe2++NH4++3H2O,
故答案为:4Fe+NO3-+10H+=4Fe2++NH4++3H2O;
②根据反应:4Fe+NO3-+10H+=4Fe2++NH4++3H2O,溶液中NH4+的浓度在增大,Fe2+的浓度却没有增大,原因是生成的Fe2+水解所致,故答案为:生成的Fe2+水解;
(3)①将铁屑和活性炭同时加入上述KNO3溶液中,活性炭和铁构成了无数个微小的铁碳原电池加快反应速率(或活性炭吸附作用,降低溶液中NH4+浓度),可以提高脱氮效果,故答案为:活性炭和铁构成了无数个微小的铁碳原电池加快反应速率(或活性炭吸附作用,降低溶液中NH4+浓度);
②根据实验原理:4Fe+NO3-+10H+=4Fe2++NH4++3H2O,在酸性环境下,金属铁的脱氮效果更加,但是CO32-+H2O?HCO3-+OH-,增大了溶液的pH会降低脱氮效果,并且Fe2++CO32-=FeCO3↓,这样碳酸亚铁沉淀覆盖在反应物的表面阻止反应进行,
故答案为:CO32-+H2O?HCO3-+OH-,增大了溶液的pH会降低脱氮效果,且Fe2++CO32-=FeCO3↓,覆盖在反应物的表面阻止反应进行.
点评:本题涉及含氮物质的综合考查题,综合性强,注意知识的迁移和应用是关键,难度中等.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
室温下,甲、乙两烧杯均盛有5mL pH=3的某一元酸溶液,向乙烧杯中加水稀释至pH=4.关于甲、乙两烧杯中溶液的描述正确的是( )
| A、溶液的体积:10V甲≤V乙 |
| B、水电离出的OH-浓度:10c(OH-)甲≤c(OH-)乙 |
| C、若分别用等浓度的NaOH溶液完全中和,所得溶液的pH:甲≤乙 |
| D、若分别与5mL pH=11的NaOH溶液反应,所得溶液的pH:甲≤乙 |
下列电离方程式中,不正确的是( )
| A、NaCl═Na++Cl- |
| B、CH3COOH?CH3COO-+H+ |
| C、NH3?H2O═NH4++OH- |
| D、NaOH═Na++OH- |
 A、B、C三种物质的物质的量随时间变化的关系图.
A、B、C三种物质的物质的量随时间变化的关系图.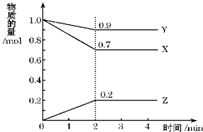 (1)在101kPa时,CO在1.0mol O2中完全燃烧,生成2.0mol CO2,放出566.0kJ的热量,则此反应的热化学方程:
(1)在101kPa时,CO在1.0mol O2中完全燃烧,生成2.0mol CO2,放出566.0kJ的热量,则此反应的热化学方程: 在一体积为10L的容器中,通入一定量的CO和H2O,850℃时发生反应:
在一体积为10L的容器中,通入一定量的CO和H2O,850℃时发生反应: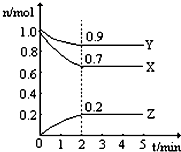 某温度时,在一个2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间的变化曲线,如图所示.根据图中数据,试填写下列空白:
某温度时,在一个2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间的变化曲线,如图所示.根据图中数据,试填写下列空白: