题目内容
某碱金属R与其氧化物R2O的混合物2.16g,跟足量水充分反应后,将所得溶液蒸干后的固体3.2g,由此判定金属是( )
| A、锂 | B、钠 | C、钾 | D、铷 |
考点:碱金属的性质,化学方程式的有关计算
专题:几种重要的金属及其化合物
分析:利用极端假设法,假设5.4g全部为金属或金属氧化物,从而确定R的相对原子质量范围,进而确定该金属的情况.
解答:
解:设该金属的相对原子质量为x,
(1)设2.16g混合物都是碱金属R,则
R~ROH
x x+17
2.16g 3.2g
=
x≈35.3
(2)设2.16g混合物都是碱金属R的氧化物R2O
则R2O~2ROH
2x+16 2x+34
2.16g 3.2g
=
x≈10.7
综(1)和(2)所述,碱金属R的相对原子质量x的范围为(10.7-35.3).在碱金属中,只有金属Na的相对分子质量23在(10.7,35.3)中,所以该碱金属是金属钠.
故选B.
(1)设2.16g混合物都是碱金属R,则
R~ROH
x x+17
2.16g 3.2g
| x |
| 2.16g |
| x+17 |
| 3.2g |
x≈35.3
(2)设2.16g混合物都是碱金属R的氧化物R2O
则R2O~2ROH
2x+16 2x+34
2.16g 3.2g
| 2x+16 |
| 2.16g |
| 2x+34 |
| 3.2g |
x≈10.7
综(1)和(2)所述,碱金属R的相对原子质量x的范围为(10.7-35.3).在碱金属中,只有金属Na的相对分子质量23在(10.7,35.3)中,所以该碱金属是金属钠.
故选B.
点评:本题考查了钠及其化合物的有关计算,利用极端假设的方法是解决此问题的关键,侧重于考查学生分析问题和解决问题的能力,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
25℃时,水的电离达到平衡:H2O?H++OH-;△H>0,下列叙述正确的是( )
| A、向平衡体系中加入水,平衡正向移动,c(OH-)增大 |
| B、将水加热,Kw增大,pH不变 |
| C、向水中加入少量稀硫酸,c (H+)增大,Kw不变 |
| D、向水中加入少量NaOH固体,平衡正向移动,c(H+)降低 |
下列实验的相关描述正确的是( )
| A、快速分离氢氧化铁胶状沉淀和氯化钠溶液可用抽滤法 |
| B、常温下,苯酚与水形成的浊液静置后会分层,上层为溶有水的苯酚溶液 |
C、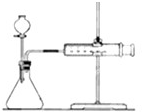 如图的装置可用于某些化学反应速率的测定.该装置气密性的检查如下:仪器组装好后,关闭分液漏斗活塞,将针筒活塞向外拉一段距离后松手,观察针筒是否能回到原来刻度处 |
| D、用氢氧化钠滴定醋酸实验,酸式滴定管没有润洗就直接使用,则所得待测液浓度偏高 |
下列叙述正确的是( )
| A、检验Fe(NO3)2试样是否变质:取少量试样加水溶解,用稀H2SO4酸化,滴加KSCN溶液 |
| B、欲鉴别AlC13溶液和AgNO3溶液,向2种待测液中分别滴加足量氨水 |
| C、将溴丙烷与足量氢氧化钠溶液混合加热,冷却后加硝酸银溶液,可检验溴元素 |
| D、用相互滴加的方法鉴别Ca(OH)2和NaHCO3溶液 |
有一块粗铝,含有铁和硅两种杂质.取两份等质量的样品分别放入足量的稀硫酸和足量的稀氢氧化钠溶液中,放出等质量的H2,则该粗铝中铁和硅的关系正确的是( )
①物质的量之比为1:2 ②物质的量之比是3:1
③质量之比是2:1 ④质量之比是4:1.
①物质的量之比为1:2 ②物质的量之比是3:1
③质量之比是2:1 ④质量之比是4:1.
| A、②④ | B、②③ | C、①④ | D、只有④ |
下列操作达到预期目的是( )
①甲烷中含有乙烯,可以通入溴水达到除去乙烯
②用酸性高锰酸钾溶液除去乙炔中含有的H2S
③用乙醇和3%的硫酸共热到170℃制取乙烯
④甲烷和氯气混合光照可以制取纯净一氯甲烷
⑤将敞口久置的电石与蒸馏水混合制乙炔.
①甲烷中含有乙烯,可以通入溴水达到除去乙烯
②用酸性高锰酸钾溶液除去乙炔中含有的H2S
③用乙醇和3%的硫酸共热到170℃制取乙烯
④甲烷和氯气混合光照可以制取纯净一氯甲烷
⑤将敞口久置的电石与蒸馏水混合制乙炔.
| A、只有① | B、只有③④⑤ |
| C、只有①②③⑤ | D、都不行 |
有4mL甲烷和一氧化碳的混合气体,完全燃烧时恰好用去了3mL的氧气,则此混合气体中甲烷和一氧化碳的体积比为( )
| A、1:1 | B、1:5 |
| C、5:1 | D、任意比 |