��Ŀ����
��830 Kʱ�����п��淴Ӧ�ﵽ�Ļ�ѧƽ����ϵ�о���ijЩ�����ԣ�CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
������ʼŨ�ȷֱ�Ϊc(CO)=3 mol��L-1,c(H2O)=0.75 mol��L-1ʱ���ﵽƽ���CO��ת����Ϊ20%��
������ʼŨ�ȷֱ�Ϊc(CO)=3 mol��L-1,c(H2O)=4.5 mol��L-1ʱ���ﵽ��ƽ���CO��ת����Ϊ60%��
��ͨ�������ͼ�������������⣺
��830 Kʱ��������ʼŨ�ȷֱ�Ϊc(CO)=a mol��L-1,c(H2O)=b mol��L-1Ͷ�ϣ��������Ϸ�Ӧ�����ƽ���c(H2)=c mol��L-1��
��1��ѡ��ش��ڶ��ʵ���У�������b�������Сa����ﵽƽ���CO��ת����____________��H2O��ת����_______________��
A.���� B.��С C.���� D.��ȷ��
��2����a=4,c=1.5ʱ��b=__________________��
��3����a=2bʱ��a��c=___________________��
��4��a��b��c�ڸ�ƽ����ϵ�еĹ�ϵʽΪ________________________��
����ʾ���ȷֱ�������������ˮ��ת���ʣ��ҳ�CO��H2Oת����֮���������ϵ��
���������¶Ȳ���ʱ�����ڿ��淴Ӧ
CO(g)+H2O(g)![]() CO2(g)+H2(g)��
CO2(g)+H2(g)��
�ٵ�cʼ(CO)=3 mol��L-1��cʼ(H2O)=0.75 mol��L-1ʱ����ƽ���CO��ת����Ϊ20%����H2O��ת����Ϊ![]() ��100%=80%��
��100%=80%��
�ڵ�cʼ(CO)���䣬cʼ(H2O)=4.5 mol��L-1ʱ����ƽ���CO��ת����Ϊ60%����H2Oת����Ϊ![]() ��100%=40%��
��100%=40%��
��1�������Ϸ�����֪����c(CO)����ʱ��c(H2O)������CO��ת��������H2O��ת���ʼ�С�������ߵ�ת����֮�ͱ��ֲ��䣬����1��ͬ����c(H2O)����ʱ��c(CO)������CO��ת���ʼ�С��H2O��ת���������ߵ�ת����֮���Ա��ֲ��䡣
��2����cʼ(CO)=4 mol��L-1ʱ��CO��ת����Ϊ![]() ��100%=37.5%����
��100%=37.5%����
![]()
��3��CO��ת����Ϊ![]() ��100%,H2O��ת����Ϊ
��100%,H2O��ת����Ϊ![]() ��100%,��Ϊ
��100%,��Ϊ![]() ��100%+
��100%+![]() ��100%=1,����c=
��100%=1,����c=![]() a��a��c=3��1��
a��a��c=3��1��
��4��![]() +
+![]() =1��
=1��
�𰸣���1��A B
��2��2.4
��3��3��1
��4��![]() +
+![]() =1
=1

 ��һ����ͬ���ɽ�����ϵ�д�
��һ����ͬ���ɽ�����ϵ�д� ������Ӧ���ϵ�д�
������Ӧ���ϵ�д� ��ʦ�㾦�ִʾ��ƪϵ�д�
��ʦ�㾦�ִʾ��ƪϵ�д� H2+CO2����ʼŨ��[CO]Ϊ2mol/L��[H2O]= 3mol/L����Ӧ�ﵽƽ��ʱ��CO��ת����Ϊ60%�������H2O����ʼŨ�ȼӴ�6mol/L����CO��ת����Ϊ75%����ע�������й����ݣ����ܽ�����ɣ�����������⣺
H2+CO2����ʼŨ��[CO]Ϊ2mol/L��[H2O]= 3mol/L����Ӧ�ﵽƽ��ʱ��CO��ת����Ϊ60%�������H2O����ʼŨ�ȼӴ�6mol/L����CO��ת����Ϊ75%����ע�������й����ݣ����ܽ�����ɣ�����������⣺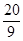 ʱ��b=
ʱ��b=
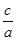 =
=