题目内容
A、B、C、D都是10电子粒子
(1)A为中性粒子.如果A能刻蚀玻璃,则A是 (写化学式,下同);如果A溶液呈碱性,则A是
(2)B为带电粒子.如果B为阳离子,且水溶液是紫色石蕊变红色,则B是 ;如果B为阴离子,且其水溶液时无色酚酞变红色,则B是
(3)C粒子中含有5个原子,带正电荷,遇碱放出NH3,C为
(4)D粒子遇阴离子B,先生成沉淀,后沉淀溶解,D是 .
(1)A为中性粒子.如果A能刻蚀玻璃,则A是
(2)B为带电粒子.如果B为阳离子,且水溶液是紫色石蕊变红色,则B是
(3)C粒子中含有5个原子,带正电荷,遇碱放出NH3,C为
(4)D粒子遇阴离子B,先生成沉淀,后沉淀溶解,D是
考点:无机物的推断
专题:
分析:常见的10电子粒子有Na+、Mg2+、Al3+、NH4+、H3O+、N3-、O2-、F-、OH-、NH2-、Ne、HF、H2O、NH3、CH4等,根据这些粒子的性质和结构可知,
(1)A为中性粒子且A能刻蚀玻璃,则A是HF,如果A溶液呈碱性,则A是NH3;
(2)B为带电粒子,如果B为阳离子,且水溶液是紫色石蕊变红色,说明B离子的水溶液呈酸性,如果B为阴离子,且其水溶液使无色酚酞变红色,说明B离子水溶液呈碱性,据此判断;
(3)遇碱放出NH3的一般是铵盐遇到碱,结合C粒子中含有5个原子可判断;
(4)先生成沉淀,后沉淀溶解,一般与反应物的量有关,结合上面的常见10电子微粒可判断.
(1)A为中性粒子且A能刻蚀玻璃,则A是HF,如果A溶液呈碱性,则A是NH3;
(2)B为带电粒子,如果B为阳离子,且水溶液是紫色石蕊变红色,说明B离子的水溶液呈酸性,如果B为阴离子,且其水溶液使无色酚酞变红色,说明B离子水溶液呈碱性,据此判断;
(3)遇碱放出NH3的一般是铵盐遇到碱,结合C粒子中含有5个原子可判断;
(4)先生成沉淀,后沉淀溶解,一般与反应物的量有关,结合上面的常见10电子微粒可判断.
解答:
解:常见的10电子粒子有Na+、Mg2+、Al3+、NH4+、H3O+、N3-、O2-、F-、OH-、NH2-、Ne、HF、H2O、NH3、CH4等,根据这些粒子的性质和结构可知,
(1)A为中性粒子且A能刻蚀玻璃,则A是HF,如果A溶液呈碱性,则A是NH3,
故答案为:HF;NH3;
(2)B为带电粒子,如果B为阳离子,且水溶液是紫色石蕊变红色,说明B离子的水溶液呈酸性,则B是Al3+或NH4+;如果B为阴离子,且其水溶液使无色酚酞变红色,说明B离子水溶液呈碱性,则B是OH-或NH2-,
故答案为:Al3+或NH4+;OH-或NH2-;
(3)C粒子中含有5个原子,带正电荷,遇碱放出NH3,则C为NH4+,故答案为:NH4+;
(4)D粒子遇阴离子B,先生成沉淀,后沉淀溶解,应该是Al3+遇到OH-,先生成氢氧化铝沉淀,氢氧化铝再溶于强碱溶液,所以D是Al3+,故答案为:Al3+.
(1)A为中性粒子且A能刻蚀玻璃,则A是HF,如果A溶液呈碱性,则A是NH3,
故答案为:HF;NH3;
(2)B为带电粒子,如果B为阳离子,且水溶液是紫色石蕊变红色,说明B离子的水溶液呈酸性,则B是Al3+或NH4+;如果B为阴离子,且其水溶液使无色酚酞变红色,说明B离子水溶液呈碱性,则B是OH-或NH2-,
故答案为:Al3+或NH4+;OH-或NH2-;
(3)C粒子中含有5个原子,带正电荷,遇碱放出NH3,则C为NH4+,故答案为:NH4+;
(4)D粒子遇阴离子B,先生成沉淀,后沉淀溶解,应该是Al3+遇到OH-,先生成氢氧化铝沉淀,氢氧化铝再溶于强碱溶液,所以D是Al3+,故答案为:Al3+.
点评:本题考查了常见10电子微粒的性质及应用,主要考查离子反应的结构特征,熟悉10电子微粒是解题关键,题目难度中等.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
下列物质中,可用重结晶法提纯的是( )
| A、含杂质的粗苯甲酸 |
| B、含杂质的工业酒精 |
| C、从溴水中提纯溴 |
| D、苯中混有少量苯酚 |
下列不能直接用乙烯为原料制取的物质是( )
| A、CH3CH2Cl |
| B、CH2Cl-CH2Cl |
C、 |
D、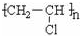 |
在反应A(g)+2B(g)?3C(g)+4D(g)中,表示该反应速率最快的是( )
| A、v(A)=0.5mol?(L?s)-1 |
| B、v(B)=0.5mol?(L?s)-1 |
| C、v(C)=0.8mol?(L?s)-1 |
| D、v(D)=1mol?(L?s)-1 |
下列各反应中属于加成反应的是( )
A、CH2=CH2+H2-OH
| ||||
B、H2+Cl2
| ||||
C、C2H4+3O2
| ||||
D、CH3-CH3+2Cl2
|
如图为氢氧燃料电池示意图,按此图的提示,下列叙述不正确的是( )


| A、a电极是负极,b电极是正极 |
| B、不管燃料电池的电解液是酸性的还是碱性的,放电后电解质溶液的pH不变 |
| C、当电解质溶液为碱性时,b电极发生的电极反应为:O2+2H2O+4e-═4OH- |
| D、氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 |
