题目内容
8.某元素的原子结构示意图为 ,有关该元素的说法中,错误的是( )
,有关该元素的说法中,错误的是( )| A. | 原子的核内质子数为17 | B. | 原子的核外有3个电子层 | ||
| C. | 原子的最外层电子数为7 | D. | 属于金属元素 |
分析 原子核外有3个电子层,最外层电子数为7,为Cl元素,位于周期表第三周期 VII族,以此解答该题.
解答 解:A、原子核外有3个电子层,最外层电子数为7,原子核内质子数为17,故A正确;
B、位于周期表第三周期,原子的核外有3个电子层,故B正确;
C、第三周期 VII族,原子的最外层电子数为7,故C正确;
D、该元素为氯,典型的非金属元素,而不是非金属元素,故D错误;
故选D.
点评 本题考查原子的结构与元素的性质,为高频考点,侧重于学生的分析能力的考查,注意把握原子的结构与元素周期率、周期表的关系,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.${\;}_{55}^{137}$Cs是核反应堆的常见放射性副产物,${\;}_{55}^{137}$Cs能自发转化为${\;}_{56}^{137}$Ba,同时放出射线.下列有关叙述正确的是( )
| A. | ${\;}_{55}^{137}$Cs与${\;}_{56}^{137}$Ba互为同位素 | |
| B. | ${\;}_{55}^{137}$Cs与${\;}_{56}^{137}$Ba中子数相等 | |
| C. | ${\;}_{56}^{137}$Ba原子最外层电子数为2 | |
| D. | Ba比Cs更容易失去电子 |
19.已知HA、H2B为二种弱酸,HA的电离常数为KHA,H2B的电离常数为K1、K2,其大小依次是K1>KHA>K2,由此可以推测以下各反应中不能进行的是( )
| A. | NaA+H2B→NaHB+HA | B. | 2NaA+H2B→Na2B+2HA | ||
| C. | NaHB+HA→NaA+H2B | D. | Na2B+HA→NaHB+NaA |
16.下列说法不正确的是( )
| A. | 向Na2CO3溶液中逐滴加入HCl,直到不再生成CO2气体为止,在此过程中,溶液中HCO3-的浓度变化是先变大后变小(溶液体积变化均忽略不计) | |
| B. | 向NaHCO3溶液中加入Ba(OH)2固体,CO32-的浓度变化是先变大后变小(溶液体积变化均忽略不计) | |
| C. | 有含0.2molNa2CO3和含0.3molHCl的两种溶液:①将Na2CO3溶液逐滴滴入HCl溶液中;②将HCl溶液逐滴滴入Na2CO3溶液中.①②两种操作生成CO2的体积之比为3:2 | |
| D. | 将等质量的Na2O和Na2O2样品分别放入等量的水中,所得溶液的质量分数分别为a%和b%,则a、b的关系是a=b |
3.下列与化学概念有关的说法正确的是( )
| A. | 化合反应均为氧化还原反应 | B. | 金属氧化物均为碱性氧化物 | ||
| C. | 烧碱、纯碱、熟石灰都是碱 | D. | BaSO4、NaOH、HNO3都是强电解质 |
13.若元素X、Y是同主族,X元素最高价氧化物对应水化物的碱性比Y强,下列有关X、Y元素及其单质和化合物的性质判断正确的是( )
| A. | 原子半径:X>Y | |
| B. | 失电子能力:X<Y | |
| C. | 对应简单离子的氧化性:X>Y | |
| D. | X元素的单质跟酸反应置换出氢气比Y容易 |
17.化学与生产、生活、社会密切相关,下列有关说法正确的是( )
| A. | 光导纤维在信息领域应用越来越广泛,其主要成分是硅单质 | |
| B. | “地沟油”禁止食用,但可以用来制肥皂 | |
| C. | 明矾常用于水体杀菌消毒 | |
| D. | 中秋将至,为防止月饼等富脂食品氧化变质,常在包装袋中放入生石灰 |
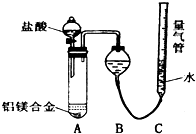 铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的三位同学,为测定某含镁3%一5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列三种不同实验方案进行探究.填写下列空白.
铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的三位同学,为测定某含镁3%一5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列三种不同实验方案进行探究.填写下列空白.