题目内容
1.用自来水养金鱼时,将水注入鱼缸以前需把水放在阳光下暴晒一段时间,目的是( )| A. | 起到杀菌作用 | B. | 使水中次氯酸分解 | ||
| C. | 提高水的温度 | D. | 增加水中氧气的含量 |
分析 普通的自来水在自来水厂都要通入氯气消毒,氯气和水反应生成盐酸和次氯酸,化学方程式:Cl2+H2O=HCl+HClO,HClO具有强氧化性,能够破坏细菌的结构,从而杀死细菌,达到消毒目的,以此来解答.
解答 解:自来水在Cl2消毒中发生Cl2+H2O?HCl+HClO,HClO 具有强氧化性,能够破坏细菌的结构,从而杀死细菌,达到消毒目的,如果将刚从自来水龙头里放出来的水直接养鱼,里面的次氯酸和盐酸就会将鱼致死,放在阳光里晒一下就是为了将次氯酸分解和使盐酸挥发出去,发生2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑,最终也就是除去水中的游离氯.
故选B.
点评 本题考查HClO的性质,为高考常见题型和高频考点,把握物质的性质、发生的反应、性质与用途为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
11.在通常条件下,下列各组物质的性质排列正确的是( )
| A. | Na、Mg、Al 的第一电离能逐渐增大 | B. | O、F、N 的电负性逐渐增大 | ||
| C. | S2-、Cl-、K+的半径逐渐增大 | D. | 热稳定性:HF>H2O>NH3 |
12.下列离子方程式,书写不正确的是( )
| A. | 大理石与盐酸反应 CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 氯化铁溶液中插入铜片:2Fe3++Cu═2Fe2++Cu2+ | |
| C. | 碳酸氢钠溶液与氢氧化钠反应:OH-+HCO3-═CO32-+H2O | |
| D. | 将铁片放入硫酸铁溶液中:Fe+Fe3+═2Fe2+ |
9.储存浓硫酸时,所用罐体的金属材料主要是( )


| A. | 镁 | B. | 银 | C. | 铁 | D. | 钠 |
16.下列有关化学用语的描述不正确的是( )
| A. | MgF2的电子式: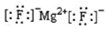 | |
| B. | 中子数为15的硅原子:${\;}_{14}^{29}$Si | |
| C. | 乙烯的结构简式:CH2CH2 | |
| D. | NH3•H2O 的电离方程式:NH3•H2O?NH4++OH- |
13.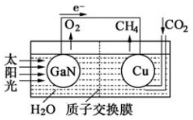 科学家用氮化镓材料与铜组装如图的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4的反应.下列说法不正确的是( )
科学家用氮化镓材料与铜组装如图的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4的反应.下列说法不正确的是( )
 科学家用氮化镓材料与铜组装如图的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4的反应.下列说法不正确的是( )
科学家用氮化镓材料与铜组装如图的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4的反应.下列说法不正确的是( )| A. | 氮化镓是一种新型无机非金属材料 | |
| B. | 铜电极表面的电极反应式:CO2+8H++8e-═CH4+2H2O | |
| C. | 溶液中H+穿过质子交换膜从左向右移动 | |
| D. | 为提高该人工光合系统的工作效率,可向装置中加入少量硫酸或盐酸 |
10.短周期元素X、Y、Z和W的原子序数依次递增,且在同一周期,四种元素原子的最外层电子数之和为19,X和Y元素原子的原子序数比6:7,X的最高正价是W的最低负价的绝对值的2倍.下列说法正确的是( )
| A. | X单质可以通过铝热法获得 | |
| B. | X的氧化物和Z的最高价氧化物化合的产物中有共价键和离子键 | |
| C. | Y的氧化物是良好的半导体材料 | |
| D. | Z的氢化物比W的氢化物更稳定 |
11.己知CO(g)+2H2(g)?CH3OH(g)是煤液化的一个反应,在温度T1和T2时将1molCO和3molH2充入2L密闭容器中测得n(CO)随时间(s)的变化如下表
下列说法正确的是( )
| 温度 n(CO) 时间 | 0 | 10 | 20 | … | 40 | 50 |
| T1 | 1.0 | 0.7 | 0.5 | … | 0.25 | 0.25 |
| T2 | 1.0 | 0.65 | 0.4 | … | 0.28 | 0.28 |
| A. | T1温度下平衡后恒容再充入0.5molCO,重新平衡后CO总的转化率与H2相等 | |
| B. | T1温度下10-20sH2的反应速率为0.04mol•L-1•s-1 | |
| C. | 该反应的△Η>0 | |
| D. | T2温度下平衡后恒定压强不变充入0.28molCH3OH,CH3OH的体积分数不变 |