题目内容
2.二氧化碳制取碳的太阳能工艺原理如图所示,下列有关说法中正确的是( )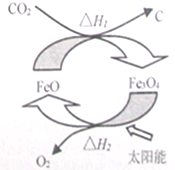
| A. | 由二氧化碳制取碳和氧气的反应为放热反应 | |
| B. | 该循环反应中,FeO的质量减小 | |
| C. | 根据盖斯定律可知,△H1+△H2=0 | |
| D. | 该反应是将太阳能转化为化学能 |
分析 A.分解反应一般为吸热反应;
B.该循环反应中,FeO作催化剂;
C.二氧化碳与FeO反应生成C和Fe3O4,Fe3O4分解生成FeO和氧气,两个反应的生成物和反应物不同;
D.反应过程中吸收太阳能.
解答 解:A.由二氧化碳制取碳和氧气的反应为分解反应,分解反应一般为吸热反应,故A错误;
B.该循环反应中,FeO作催化剂,FeO的质量保持不变,故B错误;
C.二氧化碳与FeO反应生成C和Fe3O4,Fe3O4分解生成FeO和氧气,两个反应的生成物和反应物不同,所以反应放出或吸收的热量不同,则△H1+△H2≠0,故C错误;
D.反应过程中吸收太阳能,发生了化学变化,所以反应是将太阳能转化为化学能,故D正确.
故选D.
点评 本题考查了氧化还原反应、反应热、盖斯定律的应用等,题目难度不大,注意把握题中图象所表达的含义,侧重于考查学生的分析能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.CoCl2•6H2O是一种饲料营养强化剂.一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2•6H2O的工艺流程如图:
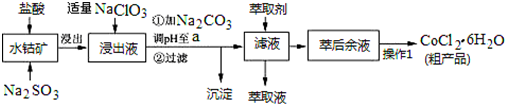
已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
③CoCl2•6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴.
(1)写出浸出过程中Co2O3发生反应的离子方程式Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)写出NaClO3发生反应的主要离子方程式ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)“加Na2CO3调pH至a”,过滤所得到的两种沉淀的化学式为Fe(OH)3、Al(OH)3.
(4)制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(5)萃取剂对金属离子的萃取率与pH的关系如图.向“滤液”中加入萃取剂的目的是除去溶液中的Mn2+;其使用的最佳pH范围是B.
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
(6)为测定粗产品中CoCl2•6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)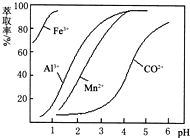

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中Co2O3发生反应的离子方程式Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)写出NaClO3发生反应的主要离子方程式ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)“加Na2CO3调pH至a”,过滤所得到的两种沉淀的化学式为Fe(OH)3、Al(OH)3.
(4)制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(5)萃取剂对金属离子的萃取率与pH的关系如图.向“滤液”中加入萃取剂的目的是除去溶液中的Mn2+;其使用的最佳pH范围是B.
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
(6)为测定粗产品中CoCl2•6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)

10.现有常温时pH=1的某强酸溶液10mL,下列操作能使溶液的pH变成2的是( )
| A. | 加入10mL 的水进行稀释 | B. | 加水稀释成100mL | ||
| C. | 加入45mL 0.01mol/L的NaOH溶液 | D. | 加入10mL 0.01mol/L的盐酸溶液 |
7.下列关于仪器使用的方法正确的是( )
| A. | 洗净的锥形瓶和容量瓶可以放进烘箱中烘干 | |
| B. | 滴定管装滴定液前应先用该溶液润洗 | |
| C. | 分液漏斗和蒸馏烧瓶使用前都要检查是否漏液 | |
| D. | 配制溶液时,只要容量瓶的容积符合要求就可以直接使用 |
14.保护环境,就是关爱自己.下列说法中你认为不正确的是( )
| A. | 空气质量日报列入的首要主要污染物有二氧化硫、二氧化氮和可吸入颗粒物等 | |
| B. | 酸雨是指pH小于7的雨水 | |
| C. | 为了减少二氧化硫和二氧化氮的排放,工业废气排放到大气之前必须进行回收处理 | |
| D. | 含磷合成洗涤剂直接排放会导致水体污染 |
11.中科院宁波材料所在金属空气电池的研发中获得重大突破.该电池的工作原理如图所示:

下列有关说法正确的是( )

下列有关说法正确的是( )
| A. | 电池工作时,负极附近溶液的pH升高 | |
| B. | 电路中转移2mol电子,理论上约消耗标准状况下空气56L | |
| C. | 电池工作时,电流由M极经外电路流向N极 | |
| D. | 电池总反应为4Al+3O2=2Al2O3、2Mg+O2=2MgO |
12.下列说法正确的是( )
| A. | 乳酸薄荷醇酯( 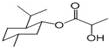 )仅能发生水解、氧化、消去反应 )仅能发生水解、氧化、消去反应 | |
| B. | 乙醛和丙烯醛( )不是同系物,它们与氢气充分反应后的产物也不是同系物 )不是同系物,它们与氢气充分反应后的产物也不是同系物 | |
| C. | 油脂在碱性条件下水解生成高级脂肪酸和甘油 | |
| D. | CH3COOCH2CH3 与CH3CH2COOCH3 互为同分异构体,1H-NMR谱显示两者均有三种不同的氢原子 |

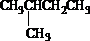

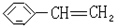 苯乙烯
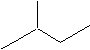
苯乙烯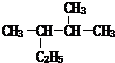 2,3-二甲基戊烷
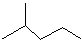
2,3-二甲基戊烷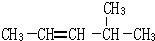 4-甲基-2戊烷
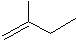
4-甲基-2戊烷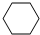 环己烷.
环己烷.