题目内容
用容量法测定磷肥含磷量的主要步骤如下:准确称取磷肥0.385g,用硫酸和高氯酸在高温下使之分解,磷转化为磷酸。过滤,洗涤,弃去残渣。以硫酸-硝酸为介质,加入过量钼酸铵溶液生成铝磷酸铵沉淀(NH4)3H4PMo12O42•H2O。过滤,洗涤,沉淀溶于40.00cm3 1.026 mol? dm-3NaOH标准溶液中,以酚酞为指示剂,用0.1022 mol?dM-3盐酸标准溶液滴定至终点(MoO42-),耗去 15.20cm3。计算磷肥中磷的百分含量(以P2O5计)。
(NH4)3H4PMo12O42?H2O+26 NaOH==12Na2MoO4+Na2HPO4+3NH3+17H2O
NH3+HCl==NH4Cl
计量关系 P2O5――(NH4)3PMo12O42?H2O――NaOH l――2――46
P2O5的摩尔质量: 142 g/mol-1
P2O5%:
(1.026mol?dm-3×0.04000dm3-0.1022mol?dm-3×0.01520dm3)×142g?mol-1/(46×0.385g)==0.317==31.7%(计量关系正确得3分,计算合理结果错扣 1分,有效数字错扣 0.5分)(6分)

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
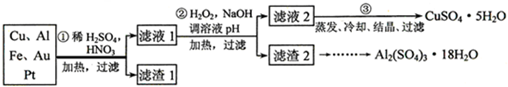
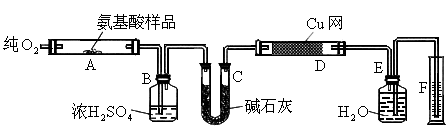
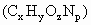 的分子组成.取Wg该种氨基酸放在纯氧气中充分燃烧,生成
的分子组成.取Wg该种氨基酸放在纯氧气中充分燃烧,生成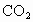 、
、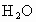 和
和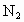 .现按图装置进行实验:
.现按图装置进行实验: