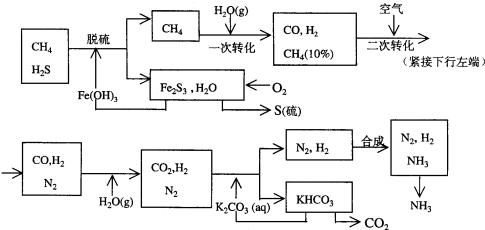
题目内容
16.下列7种物质:①白磷(P4); ②水晶; ③氯化铵; ④氢氧化钙; ⑤氟化钠; ⑥过氧化钠; ⑦干冰,固态时都为晶体,回答下列问题(填写序号):既有范德华力,又有非极性键的晶体是①,只存在离子键的是⑤,熔化时只破坏共价键的是②.
分析 分子晶体中含范德华力,同种非金属元素之间形成非极性共价键;
含离子键或离子的晶体为离子晶体,一般来说,活泼金属与非金属形成离子键;
分子晶体熔化克服分子间作用力,离子晶体熔化破坏离子键,原子晶体熔化只破坏共价键.
解答 解:①白磷(P4)属于分子晶体,只含磷磷键,既有范德华力,又有非极性键;
②水晶主要成分为二氧化硅,属于原子晶体,熔化时只破坏共价键;
③氯化铵有离子键和极性共价键,熔化破坏离子键;
④氢氧化钙有离子键和极性共价键,熔化破坏离子键;
⑤氟化钠有离子键,熔化破坏离子键;
⑥过氧化钠中有离子键和非极性共价键,熔化破坏离子键;
⑦干冰为固态二氧化碳,熔化破坏分子间作用力;
故答案为:①;⑤;②.
点评 本题主要考查化学键、晶体类型,把握化学键与晶体判断的一般规律即可解答,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案
相关题目
6. 某学生用NaOH标准溶液滴定未知浓度的盐酸,进项了如下实验:
某学生用NaOH标准溶液滴定未知浓度的盐酸,进项了如下实验:
Ⅰ.实验步骤:(请填空)
(1)滴定管在使用前应先检验是否漏液,然后用蒸馏水洗涤,最后用待装液润洗.
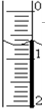
(2)将氢氧化钠溶液装入滴定管排除气泡并调节液面.如果页面初始位置如图所示,则此时的读数为0.70mL.
(3)取15.00mL待测盐酸装入锥形瓶中,滴加2滴酚酞作指示剂,滴定是边滴边摇动锥形瓶,眼睛应观察b(选填编号).
a.滴定管内液面的变化 b.锥形瓶内溶液颜色的变化
Ⅱ.实验记录:
(4)请填写1组反应消耗的氢氧化钠溶液体积.
Ⅲ.数据处理与讨论:
(5)处理数据时应舍去误差明显过大的异常数据,余下的数据中NaOH溶液的平均消耗值是16.00mL.若
NaOH标准溶液的浓度为0.1020mol/L,该盐酸的浓度为0.1088mol/L.
(6)在本实验过程中,下列操作不会造成实验误差的是a(选填编号).
a.锥形瓶中加入待测溶液后,再加少量蒸馏水
b.锥形瓶在滴定时剧烈摇动,有少量液体溅出
c.见到指示剂的颜色有变化即停止滴定.
 某学生用NaOH标准溶液滴定未知浓度的盐酸,进项了如下实验:
某学生用NaOH标准溶液滴定未知浓度的盐酸,进项了如下实验:Ⅰ.实验步骤:(请填空)
(1)滴定管在使用前应先检验是否漏液,然后用蒸馏水洗涤,最后用待装液润洗.
(2)将氢氧化钠溶液装入滴定管排除气泡并调节液面.如果页面初始位置如图所示,则此时的读数为0.70mL.
(3)取15.00mL待测盐酸装入锥形瓶中,滴加2滴酚酞作指示剂,滴定是边滴边摇动锥形瓶,眼睛应观察b(选填编号).
a.滴定管内液面的变化 b.锥形瓶内溶液颜色的变化
Ⅱ.实验记录:
| 实验次数 | 待测盐酸体积(mL) | 标准氢氧化钠溶液体积(mL) | ||
| 初读数 | 末读数 | 消耗体积 | ||
| 1 | 15.00 | 0.50 | 17.75 | 17.25 |
| 2 | 15.00 | 0.05 | 16.10 | 16.05 |
| 3 | 15.00 | 0.00 | 15.95 | 15.95 |
Ⅲ.数据处理与讨论:
(5)处理数据时应舍去误差明显过大的异常数据,余下的数据中NaOH溶液的平均消耗值是16.00mL.若
NaOH标准溶液的浓度为0.1020mol/L,该盐酸的浓度为0.1088mol/L.
(6)在本实验过程中,下列操作不会造成实验误差的是a(选填编号).
a.锥形瓶中加入待测溶液后,再加少量蒸馏水
b.锥形瓶在滴定时剧烈摇动,有少量液体溅出
c.见到指示剂的颜色有变化即停止滴定.
7.下列物质中只含有共价键的是( )
| A. | HBr、CO2、H2O、CS2 | B. | Cl2、Na2S、HCl、SO2 | ||
| C. | NaCl、HCl、H2O、NaOH | D. | Na2O2、H2O2、H2O、O3 |
4.下列说法正确的是( )
| A. | 反应物具有的总能量总是高于生成物所具有总能量 | |
| B. | 需要加热方能发生的反应一定是吸热反应 | |
| C. | 构成原电池的正极和负极必须是两种不同的金属 | |
| D. | 决定化学反应速率的主要因素是参加反应的物质的性质 |
1. 布洛芬属于丁苯丙酸的一种,是世界卫生组织推荐的獐抗炎退烧药,其结构如图所示.下列说法不正确的是( )
布洛芬属于丁苯丙酸的一种,是世界卫生组织推荐的獐抗炎退烧药,其结构如图所示.下列说法不正确的是( )
 布洛芬属于丁苯丙酸的一种,是世界卫生组织推荐的獐抗炎退烧药,其结构如图所示.下列说法不正确的是( )
布洛芬属于丁苯丙酸的一种,是世界卫生组织推荐的獐抗炎退烧药,其结构如图所示.下列说法不正确的是( )| A. | 布洛芬的分子式为C12H18O2 | B. | 布洛芬与苯丙酸互为同系物 | ||
| C. | 丁苯丙酸共有12种可能的结构 | D. | 布洛芬能发生加成、取代等反应 |
5.由3-甲基-2-戊烯、葡萄糖、丙酸、丁酸乙酯组成的混合物中,测得氢元素的质量分数为9%,则混合物中氧元素的质量分数为( )
| A. | 30% | B. | 37% | ||
| C. | 50% | D. | 数据不全无法计算 |
6.下列解释实验事实的化学方程式或离子方程式正确的是( )
| A. | 用pH试纸检测,氨水溶液呈碱性:NH3•H2O=NH4++OH- | |
| B. | 100℃时,测得纯水中c(H+)•c(OH-)=3.8×10-13 H2O(l)?H+(aq)+OH-(aq)△H<0 | |
| C. | FeCl3溶液中通入适量SO2,溶液黄色褪去:Fe3++SO2+2H2O=Fe2++SO42-+4H+ | |
| D. | 用CaSO4治理盐碱地:CaSO4(s)+Na2CO3(aq)?CaCO3(s)+Na2SO4(aq) |