题目内容
13.某溶液中大量存在以下五种离子NO3-、SO42-、Al3+、H+、M.其物质的量浓度之比为c(NO3-):c(SO42-):c(Al3+):c(H+):c(M)=4:3:1:3:2,则M可能是( )| A. | Fe2+ | B. | Cl- | C. | Mg2+ | D. | Ba2+ |
分析 由于Ba2+与SO42-反应生成BaSO4沉淀,则M不可能为Ba2+,酸性条件下NO3-可以氧化Fe2+,则M也不可能为Fe2+,再根据电荷守恒判断.
解答 解:由于Ba2+与SO42-反应生成BaSO4沉淀,则M不可能为Ba2+,酸性条件下NO3-可以氧化Fe2+,则M也不可能为Fe2+,
设c(NO3-)、c(S042-)、c(Al3+)、c(H+)、c(M)分别为4mol/L、3mol/L、1mol/L、3mol/L、2mol/L,由电荷守恒可知:3c(Al3+)+c(H+)=6mol/L<c(NO3-)+2c(S042-)=10mol/L,故M为阳离子,且M所得电荷数为$\frac{10mol/L-6mol/L}{2mol/L}$=2,故选项中Mg2+符合,
故选:C.
点评 本题考查物质的量浓度计算、离子共存问题,题目难度中等,注意根据电荷守恒判断M应为阳离子,属于易错题目,学生容易考虑电荷守恒,忽略离子共存问题.

练习册系列答案
相关题目
8.进行化学实验时应强化安全意识.下列做法正确的是( )
| A. | 用试管加热碳酸氢钠固体时使试管口竖直向上 | |
| B. | 金属钠着火时使用泡沫灭火器灭火 | |
| C. | 验证氯气能否与水反应的实验时,用氢氧化钠溶液处理尾气 | |
| D. | 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 |
18.下列有关实验现象的叙述中,不正确的是( )
| A. | 氢气在Cl2中燃烧,产生苍白色火焰,瓶口有白雾生成 | |
| B. | 铁丝在Cl2中燃烧,产生棕红色的烟 | |
| C. | 钠在Cl2中燃烧,生成白色的雾 | |
| D. | 铜丝在Cl2中燃烧,生成棕黄色的烟 |
5.关于氧化物的叙述正确的是( )
| A. | 非金属氧化物一定是酸性氧化物 | B. | 碱性氧化物一定是金属氧化物 | ||
| C. | 碱性氧化物都能与水化合生成碱 | D. | 酸性氧化物都能与水化合生成酸 |
2.关于SO2下列变化和其性质对应关系正确的是( )
| A. | 品红溶液褪色---漂白性 | B. | 高锰酸钾溶液褪色---漂白性 | ||
| C. | 导致酸雨---酸性氧化物 | D. | 通入H2S溶液中变浑浊---氧化性 |
3.废弃物的综合利用既有利于节约资源,又有利于保护环境.实验室利用废旧电池的铜帽(Cu、Zn 总含量约为99%)回收Cu并制备ZnO 的部分实验过程如下: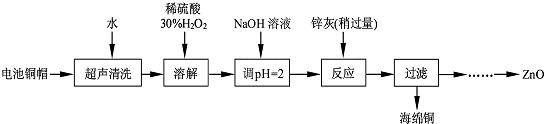
(1)写出铜帽溶解时铜与加入的稀硫酸、30%H2O2 反应的离子反应方程式Cu+H2O2+2H+=Cu2++2H2O;铜帽溶解完全后,需加热(至沸)将溶液中过量的H2O2除去.
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H2O2 后溶液中Cu2+的含量.实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用Na2S2O3标准溶液滴定至终点.上述过程中反应的离子方程式如下:
2Cu2++4I-═2CuI(白色)↓+I2 2S2O32-+I2═2I-+S4O62-
①滴定选用的指示剂为淀粉溶液,滴定终点观察到的现象为蓝色褪去;
②某同学称取1.0g电池铜帽进行实验,得到100.00mL含有Cu2+的溶液,量取20.00mL上述含有
Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用0.1000mol/L Na2S2O3标准溶液滴定至终点.再重复操作实验3次,记录数据如下:
计算电池铜帽中Cu的质量分数为80.99%,(结果保留四位有效数字)若滴定前溶液中的H2O2没有除
尽,则所测定c (Cu2+)将会偏大(填“偏高”、“偏低”或“无影响”);
(3)常温下,若向50mL 0.0001mol/L CuSO4溶液中加入50mL0.00022mol/LNaOH溶液,生成了沉淀.已知KSP[Cu (OH)2]=2.0×10-20(mol/L)3,计算沉淀生成后溶液中c(Cu2+)=2×10-10mol/L;
(4)已知pH>11 时Zn(OH)2 能溶于NaOH溶液生成[Zn(OH)4]2-.下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH 按金属离子浓度为1.0mol•L-1计算).
实验中可选用的试剂:30%H2O2、1.0mol•L-1HNO3、1.0mol•L-1NaOH.由除去铜的滤液制备ZnO 的实验步骤依次为:①向滤液中加入适量30% H2O2,使其充分反应;
②滴加1.0mol•L-1NaOH,调节溶液PH约为5(或3.2≤pH<5.9),使Fe3+沉淀完全;③过滤;
④向滤液中滴加1.0mol•L-1NaOH,调节溶液PH约为10(或8.9≤pH≤11),使Zn2+沉淀完全;⑤过滤、洗涤、干燥;⑥900℃煅烧.

(1)写出铜帽溶解时铜与加入的稀硫酸、30%H2O2 反应的离子反应方程式Cu+H2O2+2H+=Cu2++2H2O;铜帽溶解完全后,需加热(至沸)将溶液中过量的H2O2除去.
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H2O2 后溶液中Cu2+的含量.实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用Na2S2O3标准溶液滴定至终点.上述过程中反应的离子方程式如下:
2Cu2++4I-═2CuI(白色)↓+I2 2S2O32-+I2═2I-+S4O62-
①滴定选用的指示剂为淀粉溶液,滴定终点观察到的现象为蓝色褪去;
②某同学称取1.0g电池铜帽进行实验,得到100.00mL含有Cu2+的溶液,量取20.00mL上述含有
Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用0.1000mol/L Na2S2O3标准溶液滴定至终点.再重复操作实验3次,记录数据如下:
| 实验编号 | 1 | 2 | 3 | 4 |
| V(Na2S2O3)(mL) | 28.32 | 25.31 | 25.30 | 25.32 |
尽,则所测定c (Cu2+)将会偏大(填“偏高”、“偏低”或“无影响”);
(3)常温下,若向50mL 0.0001mol/L CuSO4溶液中加入50mL0.00022mol/LNaOH溶液,生成了沉淀.已知KSP[Cu (OH)2]=2.0×10-20(mol/L)3,计算沉淀生成后溶液中c(Cu2+)=2×10-10mol/L;
(4)已知pH>11 时Zn(OH)2 能溶于NaOH溶液生成[Zn(OH)4]2-.下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH 按金属离子浓度为1.0mol•L-1计算).
| 开始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
②滴加1.0mol•L-1NaOH,调节溶液PH约为5(或3.2≤pH<5.9),使Fe3+沉淀完全;③过滤;
④向滤液中滴加1.0mol•L-1NaOH,调节溶液PH约为10(或8.9≤pH≤11),使Zn2+沉淀完全;⑤过滤、洗涤、干燥;⑥900℃煅烧.
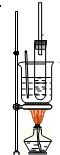 实验室制取硝基苯的方法如图所示:
实验室制取硝基苯的方法如图所示: ,
,