题目内容
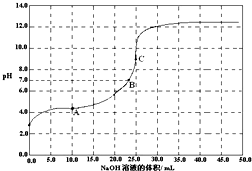 常温时,用0.1000mol/L NaOH 滴定 25.00mL 0.1000mol/L某一元酸HX,滴定过程中pH 变化曲线如图所示.下列说法正确的是( )
常温时,用0.1000mol/L NaOH 滴定 25.00mL 0.1000mol/L某一元酸HX,滴定过程中pH 变化曲线如图所示.下列说法正确的是( )| A、滴定前,酸中c(H+) 等于碱中c(OH-) |
| B、在A点,c(Na+)>c(X-)>c(HX)>c(H+)>c(OH-) |
| C、在B点,两者恰好完全反应 |
| D、在C点,c(X-)+c(HX)=0.05 mol/L |
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:A.0.1000mol/L某一元酸HX,其2<pH<4,为弱酸,c(H+)<0.1000mol/L,而NaOH为强碱,c(OH-)=0.1000mol/L;
B.在A点,显酸性,碱不足,则溶液中的溶质为HX和NaX;
C.在B点,pH=7,加入的NaOH溶液的体积小于25.00mL,溶质为HX和NaX;
D.C点,溶液的总体积为50.00mL,结合物料守恒分析.
B.在A点,显酸性,碱不足,则溶液中的溶质为HX和NaX;
C.在B点,pH=7,加入的NaOH溶液的体积小于25.00mL,溶质为HX和NaX;
D.C点,溶液的总体积为50.00mL,结合物料守恒分析.
解答:
解:A.0.1000mol/L某一元酸HX,其2<pH<4,为弱酸,c(H+)<0.1000mol/L,而NaOH为强碱,c(OH-)=0.1000mol/L,则滴定前,酸中c(H+) 不等于碱中c(OH-),故A错误;
B.在A点,显酸性,碱不足,则溶液中的溶质为HX和NaX,结合量的关系可知c(HX)>c(X-)>c(Na+)>c(H+)>c(OH-),故B错误;
C.在B点,pH=7,加入的NaOH溶液的体积小于25.00mL,溶质为HX和NaX,显然碱不足,没有恰好完全反应,故C错误;
D.C点,溶液的总体积为50.00mL,由物料守恒可知c(X-)+c(HX)=
=0.05mol/L,故D正确;
故选D.
B.在A点,显酸性,碱不足,则溶液中的溶质为HX和NaX,结合量的关系可知c(HX)>c(X-)>c(Na+)>c(H+)>c(OH-),故B错误;
C.在B点,pH=7,加入的NaOH溶液的体积小于25.00mL,溶质为HX和NaX,显然碱不足,没有恰好完全反应,故C错误;
D.C点,溶液的总体积为50.00mL,由物料守恒可知c(X-)+c(HX)=
| 0.1000mol/L×0.025L |
| 0.05L |
故选D.
点评:本题考查酸碱混合溶液中的定性判断,明确图中各点发生的化学反应及溶液中的溶质是解答本题的关键,注意物料守恒的应用及量的关系,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列解释实验现象的反应方程式正确的是( )
| A、SO2通入到滴加酚酞的NaOH溶液中,红色变浅:SO2+2NaOH=Na2SO4+H2O | ||||
| B、向K2Cr2O7溶液中加入少量NaOH浓溶液,溶液由橙色变为黄色:Cr2O72-+H2O?2CrO42-+2H+ | ||||
| C、等浓度的NH4Al(SO4)2溶液与Ba(OH)2溶液以1:2体积比混合出现白色沉淀:Al3++2SO42-+2Ba2++3OH-=2BaSO4↓+Al(OH)3↓ | ||||
D、铝热反应的原理为:Al2O3+2Fe
|
下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
| 物质 编号 |
物质转化关系 | 甲 | 乙 | 丙 | 丁 |
| ① | 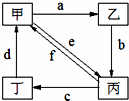 |
Cu | CuO | CuSO4 | Cu(NO3)2 |
| ② | Na2CO3 | NaOH | NaHCO3 | CO2 | |
| ③ | (NH4)2SO3 | CaSO3 | SO2 | NH4HSO3 | |
| ④ | CH3CH2Cl | C2H5OH | CH2=CH2 | CH3CH3 |
| A、①②③④ | B、①②③ |
| C、①③④ | D、②④ |
用盐酸中和相同体积、相同pH值的Ba(OH)2、NaOH和NH3?H2O三种稀溶液,所用相同浓度的盐酸体积分别为V1、V2和V3,则三者关系为( )
| A、V1>V2>V3 |
| B、V3=V2>V1 |
| C、V1=V2>V3 |
| D、V3>V2=V1 |
 某离子晶体晶胞结构如图,(●)X位于立方体的顶点,(○)Y位于立方体的中心,试分析:
某离子晶体晶胞结构如图,(●)X位于立方体的顶点,(○)Y位于立方体的中心,试分析: