题目内容
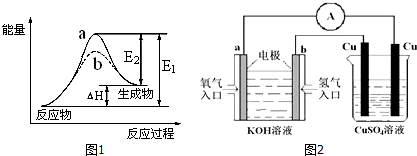
12.下列说法正确的是( )| A. | 升高温度能使化学反应速率增大,主要原因是降低了反应活化能 | |
| B. | 有气体参加的化学反应,增大压强一定可以增大化学反应速率 | |
| C. | 增大反应物浓度,可提高单位体积内活化分子的百分数,从而使有效碰撞次数增大 | |
| D. | 催化剂的加入能提高单位体积内活化分子百分数,从而增大化学反应速率 |
分析 增大浓度、压强,活化分子的浓度增大,但百分数不变,升高温度、加入催化剂,可增大活化分子的百分数,以此解答该题.
解答 解:A.温度升高,增加了反应体系中活化分子百分数,反应速率加快,故A错误;
B.如加入惰性气体,不改变参加反应气体的浓度,则速率不变,故B错误;
C.增大浓度,增加了反应体系中活化分子数目增大,但百分数不变,故C错误;
D.催化剂降低反应的活化能,增加了反应体系中活化分子百分数,则反应速率加快,故D正确.
故选D.
点评 本题考查影响反应速率的因素,为高频考点,把握活化理论与反应速率的关系为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
20.欲将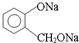 转化为
转化为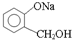 ,可以加入( )
,可以加入( )
 转化为
转化为 ,可以加入( )
,可以加入( )| A. | 水 | B. | 碳酸氢钠溶液 | C. | 碳酸 | D. | 盐酸 |
7.粗盐提纯过程中分别加入Na2CO3和BaCl2以除去CaCl2和Na2SO4,它们的添加顺序是( )
| A. | Na2CO3加在BaCl2前 | B. | Na2CO3加在BaCl2后 | ||
| C. | 同时加 | D. | 无固定顺序 |
17.下列关于浓HNO3与浓H2SO4的叙述正确的是( )
| A. | 都具有脱水性 | |
| B. | 在加热条件下都能与碳反应 | |
| C. | 露置于空气中都能形成白雾 | |
| D. | 在空气中长期露置,溶液质量均减轻 |
1.下列与化学有关的说法不正确的是( )
| A. | 洁厕灵的主要成分是盐酸,不能与“84”消毒液(主要成分是NaClO)混用 | |
| B. | 晶体的风化、煤的液化、石油的裂化都是化学变化 | |
| C. | 明矾水解时产生具有吸附性的胶体粒子,可以用于饮用水的杀菌消毒 | |
| D. | 可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气 |
2.在足量的CuSO4溶液中加入下列试剂后,溶液质量减少了8g,则加入的物质是( )
| A. | 23g金属钠 | B. | 1mol/L BaCl2溶液100mL | ||
| C. | 56g金属铁 | D. | 20% NaOH溶液50g |