题目内容
下列物质属于盐的是( )
| A、HNO3 |
| B、CuO |
| C、KOH |
| D、NaCl |
考点:酸、碱、盐、氧化物的概念及其相互联系
专题:
分析:碱是指电离时产生的阴离子全部是氢氧根离子的化合物;酸是指电离时产生的阳离子全部是氢离子的化合物;盐是指由金属离子和酸根离子组成的化合物.
解答:
解:A、硝酸能电离出的阳离子只有氢离子,故属于酸;
B、氧化铜属于金属氧化物;
C、氢氧化钾电离出的阴离子只有氢氧根,属于碱;
D、NaCl能电离出金属阳离子和酸根离子,故是盐,故选D.
B、氧化铜属于金属氧化物;
C、氢氧化钾电离出的阴离子只有氢氧根,属于碱;
D、NaCl能电离出金属阳离子和酸根离子,故是盐,故选D.
点评:本题主要考查了物质的分类,掌握酸、碱、盐、氧化物的概念是解答的关键,题目难度不大.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
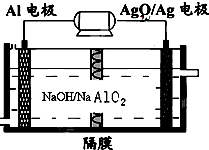 铝电池性能优越,Al-Ag2O电池可用作水下动力电源,其原理如图所示.下列说法正确的是( )
铝电池性能优越,Al-Ag2O电池可用作水下动力电源,其原理如图所示.下列说法正确的是( )| A、电池负极反应式2Ag+2OH--2e-=Ag 2O+H2O |
| B、放电时电池负极附近PH减小 |
| C、电池总反应式2Al+3Ag2O+6H+=2Al3++6Ag+3H2O |
| D、电解液中Na+通过隔膜由右向左移动 |
下列有关化学用语表示正确的是( )
| A、蚁醛的最简式:CH2O | ||
B、中子数为20的氯原子:
| ||
C、氮原子最外层电子轨道表示式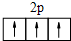 | ||
D、NH4Br的电子式 |
元素的性质呈现周期性变化的根本原因是( )
| A、原子半径呈周期性变化 |
| B、元素的化合价呈周期性变化 |
| C、第一电离能呈周期性变化 |
| D、元素原子的核外电子排布呈周期性变化 |
下列各组离子一定能大量共存的是( )
| A、含有大量Fe3+的溶液中:NH4+、Na+、Cl-、OH- |
| B、在强碱溶液中:Na+、K+、ClO-、CO32- |
| C、在强酸的溶液中:K+、Fe2+、Cl-、NO3- |
| D、在强碱的溶液中:K+、Na+、Ca2+、HCO3- |
据科学家预测,月球的土壤中吸附着数百万吨的 3He,每百吨 3He核聚变所释放出的能量相当于目前人类一年消耗的能量.在地球上,氦元素主要以 4He的形式存在.下列说法中正确的是( )
| A、4He原子核内含有4个质子 |
| B、3He和4He互为同位素 |
| C、3He原子核内含有3个中子 |
| D、4He的最外层电子数为2,故 4He具有较强的金属性 |
在反应4P+3KOH+3H2O=3KH2PO2+PH3中氧化剂与还原剂的分子个数之比为( )
| A、3:1 | B、1:3 |
| C、4:1 | D、1:4 |