题目内容
5.设NA为阿伏加德罗常数的值,下列说法错误的是( )| A. | 1mol/L 的Na2CO3溶液中,含有的Na+离子数为2 NA | |
| B. | 0.5 mol H2SO4含有的原子数目为3.5NA | |
| C. | 32 g O2所含的分子数目为NA | |
| D. | 27g金属铝变成铝离子时失去的电子数为3NA |
分析 A、溶液体积不明确;
B、硫酸为7原子分子;
C、分子个数N=$\frac{m}{M}{N}_{A}$;
D、求出铝的物质的量,然后根据铝反应后变为+3价来分析.
解答 解:A、溶液体积不明确,故溶液中的钠离子的个数无法计算,故A错误;
B、硫酸为7原子分子,故0.5mol硫酸中含3.5NA个原子,故B正确;
C、分子个数N=$\frac{m}{M}{N}_{A}$=$\frac{32g}{32g/mol}×{N}_{A}/mol$=NA个,故C正确;
D、27g铝的物质的量为1mol,而铝反应后变为+3价,故1mol铝失去3NA个电子,故D正确.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
5.Mg-AgCl电池是一种以海水为电解质溶液的水激活电池.下列叙述正确的是( )
| A. | 正极反应式为Mg-2e-═Mg2+ | |
| B. | 正极反应式为Ag+e-═Ag | |
| C. | 电池放电时Cl-由负极向正极迁移 | |
| D. | 负极会发生副反应Mg+2H2O═Mg(OH)2+H2↑ |
20.写出除杂的试剂和方法:
| 试剂 | 方 法 | |
| 乙烷中混有少量乙烯 | ||
| 苯中混有少量甲苯 | ||
| 乙醇中混有少量水 |
10.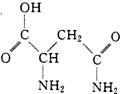 芦笋中的天冬酰胺(结构如图)和微量元素硒、铬、锰等,具有提高身体免疫力的功效.
芦笋中的天冬酰胺(结构如图)和微量元素硒、铬、锰等,具有提高身体免疫力的功效.
(1)天冬酰胺所含元素中,氮(填元素名称)元素基态原子核外未成对电子数最多.
(2)天冬酰胺中碳原子的杂化轨道类型有sp3、sp2.
(3)H2Se的晶体类型为分子晶体,含有的共价键类型为极性共价键.
(4)已知钼(Mo)位于第五周期、ⅥB族,钼、铬、锰的部分电离能如表所示:
A是Mn(填元素符号),B原子的价电子排布式为3d54s1.
 芦笋中的天冬酰胺(结构如图)和微量元素硒、铬、锰等,具有提高身体免疫力的功效.
芦笋中的天冬酰胺(结构如图)和微量元素硒、铬、锰等,具有提高身体免疫力的功效.(1)天冬酰胺所含元素中,氮(填元素名称)元素基态原子核外未成对电子数最多.
(2)天冬酰胺中碳原子的杂化轨道类型有sp3、sp2.
(3)H2Se的晶体类型为分子晶体,含有的共价键类型为极性共价键.
(4)已知钼(Mo)位于第五周期、ⅥB族,钼、铬、锰的部分电离能如表所示:
| 编号 | I5/kJ•mol-1 | I6/kJ•mol-1 | I7/kJ•mol-1 | I8/kJ•mol-1 |
| A | 6990 | 9220 | 11500 | 18700 |
| B | 6702 | 8745 | 15455 | 17820 |
| C | 5257 | 6641 | 12125 | 13860 |
17.化学与生活、社会密切相关.“低碳经济,节能减排”是今后经济发展的新思路.下列说法不正确的是( )
| A. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 | |
| B. | 将废弃的秸秆转化为清洁高效的能源 | |
| C. | 为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 | |
| D. | 采用新技术开采煤、石油和天然气,以满足经济发展的需要 |
15.与OH-具有相同质子数和电子数的粒子是( )
| A. | H2O | B. | F- | C. | Na+ | D. | NH3 |