题目内容
根据下列热化学方程式:①C(s)+O2(g)===CO2(g) ΔH1=-393.5 kJ/mol
②H2(g)+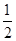 O2(g)===H2O(l) ΔH2=-285.8 kJ/mol
O2(g)===H2O(l) ΔH2=-285.8 kJ/mol
③CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH 3=-870.3 kJ/mol
可以计算出2C(s)+2H2(g)+O2(g)===CH3COOH(l)的反应热为
A.ΔH =+244.1 kJ/mol B.ΔH =-488.3 kJ/mol
C.ΔH =-996.6 kJ/mol D.ΔH =+996.6 kJ/mol
【答案】
B
【解析】
试题分析:根据盖斯定律,为了求出总反应:2C(s)+2H2(g)+O2(g)===CH3COOH(l) ,可以把①②③三个反应可以综合在一起,①×2+②×2-③即是总反应,则反应热也随之相加减,可以求出ΔH =2×ΔH1+2×ΔH2-ΔH 3=-488.3 kJ/mol
考点:热化学方程式的意义及盖斯定律的应用。
点评:本题需要学生对盖斯定律的内容会熟练运用,涉及到计算是学生的一个难点,所以本题属于中档题。

练习册系列答案
相关题目
 O2(g)
= H2O(l)
△H2=–285.8 kJ/mol
O2(g)
= H2O(l)
△H2=–285.8 kJ/mol