题目内容
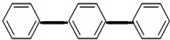
 (1)某芳香烃结构如图所示:它的分子式为
(1)某芳香烃结构如图所示:它的分子式为C18H14
C18H14
,一氯代物有4
4
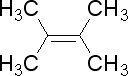
种.(2)(CH3CH2)2C(CH3)2的系统命名为
3,3-二甲基戊烷
3,3-二甲基戊烷
.(3)某烃分子中碳氢质量比为6:1,其实验式为
CH2
CH2
;又测得该化合物对氢气的相对密度为14,该化合物的分子式为C2H4
C2H4
.(4)写出3P轨道有1个未成对电子的元素符号:
Cl
Cl
.分析:(1)基本解法等效氢法:①同一碳原子上的氢原子等效;②同一碳原子上所连-CH3上的氢原子等效;③处于对称位置上的碳原子上的氢原子等效;有几类氢原子就有几种一氯代物;
(2)烷烃命名原则:
①长-----选最长碳链为主链;
②多-----遇等长碳链时,支链最多为主链;
③近-----离支链最近一端编号;
④小-----支链编号之和最小.看下面结构简式,从右端或左端看,均符合“近-----离支链最近一端编号”的原则;
⑤简-----两取代基距离主链两端等距离时,从简单取代基开始编号.如取代基不同,就把简单的写在前面,复杂的写在后面;
(3)实验式是化学式的一种.用元素符号表示化合物分子中元素的种类和各元素原子个数的最简整数比的式子;根据分子式计算原子个数比解得实验式;根据相对分子质量和质量比可求出化学式;
(4)p能级有3个轨道,3p轨道上有1个未成对电子,则3p能级为3p5;
核外电子排布规律:
1、泡利不相容原理:每个轨道最多只能容纳两个电子,且自旋相反配对.
2、能量最低原理:电子尽可能占据能量最低的轨道,符合构造原理.
3、洪特规则:简并轨道(能级相同的轨道)只有被电子逐一自旋平行地占据后,才能容纳第二个电子另外:等价轨道在全充满、半充满或全空的状态是比较稳定的,亦即下列电子结构是比较稳定.
(2)烷烃命名原则:
①长-----选最长碳链为主链;
②多-----遇等长碳链时,支链最多为主链;
③近-----离支链最近一端编号;
④小-----支链编号之和最小.看下面结构简式,从右端或左端看,均符合“近-----离支链最近一端编号”的原则;
⑤简-----两取代基距离主链两端等距离时,从简单取代基开始编号.如取代基不同,就把简单的写在前面,复杂的写在后面;
(3)实验式是化学式的一种.用元素符号表示化合物分子中元素的种类和各元素原子个数的最简整数比的式子;根据分子式计算原子个数比解得实验式;根据相对分子质量和质量比可求出化学式;
(4)p能级有3个轨道,3p轨道上有1个未成对电子,则3p能级为3p5;
核外电子排布规律:
1、泡利不相容原理:每个轨道最多只能容纳两个电子,且自旋相反配对.
2、能量最低原理:电子尽可能占据能量最低的轨道,符合构造原理.
3、洪特规则:简并轨道(能级相同的轨道)只有被电子逐一自旋平行地占据后,才能容纳第二个电子另外:等价轨道在全充满、半充满或全空的状态是比较稳定的,亦即下列电子结构是比较稳定.
解答:解:(1)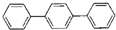 的分子式为C18H14,根据等效氢法:①同一碳原子上的氢原子等效;②同一碳原子上所连-CH3上的氢原子等效;③处于对称位置上的碳原子上的氢原子等效;有4类氢原子就有四种一氯代物,故答案为:C18H14;4;
的分子式为C18H14,根据等效氢法:①同一碳原子上的氢原子等效;②同一碳原子上所连-CH3上的氢原子等效;③处于对称位置上的碳原子上的氢原子等效;有4类氢原子就有四种一氯代物,故答案为:C18H14;4;
(2)(CH3CH2)2C(CH3)2的系统命名,选取含最多碳原子的为主碳链,主链上有五个碳原子,从离取代基最近的一端起编号,写出名称,3,3-二甲基戊烷,
故答案为:3,3-二甲基戊烷;
(3)碳氢质量比为6:1,碳氢原子个数的最简整数比为1:2,
该化合物对氢气的相对密度为14,则该化合物的分子量,14×2=28,设该化合物的化学式为CxHy.
12x:y=6:1
12x+y=28
解得:x=2,y=4,
因此该化合物的化学式为C2H4,
故答案为:CH2;C2H4;
(4)p能级有3个轨道,3p轨道上有1个未成对电子,则3p能级为3p5,即电子排布式为1s22s22p63s23p5,故为Cl,故答案为:Cl.
 的分子式为C18H14,根据等效氢法:①同一碳原子上的氢原子等效;②同一碳原子上所连-CH3上的氢原子等效;③处于对称位置上的碳原子上的氢原子等效;有4类氢原子就有四种一氯代物,故答案为:C18H14;4;
的分子式为C18H14,根据等效氢法:①同一碳原子上的氢原子等效;②同一碳原子上所连-CH3上的氢原子等效;③处于对称位置上的碳原子上的氢原子等效;有4类氢原子就有四种一氯代物,故答案为:C18H14;4;(2)(CH3CH2)2C(CH3)2的系统命名,选取含最多碳原子的为主碳链,主链上有五个碳原子,从离取代基最近的一端起编号,写出名称,3,3-二甲基戊烷,
故答案为:3,3-二甲基戊烷;
(3)碳氢质量比为6:1,碳氢原子个数的最简整数比为1:2,
该化合物对氢气的相对密度为14,则该化合物的分子量,14×2=28,设该化合物的化学式为CxHy.
12x:y=6:1
12x+y=28
解得:x=2,y=4,
因此该化合物的化学式为C2H4,
故答案为:CH2;C2H4;
(4)p能级有3个轨道,3p轨道上有1个未成对电子,则3p能级为3p5,即电子排布式为1s22s22p63s23p5,故为Cl,故答案为:Cl.
点评:本题考查了分子式书写,等效氢的判断,实验式,物质的命名方法,掌握等效氢的判断是解题关键,题目较简单.

练习册系列答案
相关题目
 (1)某芳香烃结构如图:它的分子式为
(1)某芳香烃结构如图:它的分子式为