题目内容
3.能正确表示下列反应的离子方程式是( )| A. | 将铜屑加入Fe3+溶液中:2Fe3++Cu═2Fe2++Cu2+ | |
| B. | 将磁性氧化铁溶于盐酸:Fe3O4+8H+═3Fe3++4H2O | |
| C. | 氯化亚铁溶液中通入氯气:Fe2++Cl2═Fe3++2Cl- | |
| D. | 将铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ |
分析 A.遵循电子、电荷守恒;
B.反应生成氯化铁、氯化亚铁和水;
C.电子、电荷不守恒;
D.反应生成硫酸亚铁和氢气.
解答 解:A.将铜屑加入Fe3+溶液中的离子反应为2Fe3++Cu═2Fe2++Cu2+,故A正确;
B.将磁性氧化铁溶于盐酸的离子反应为Fe3O4+8H+═Fe2++2Fe3++4H2O,故B错误;
C.氯化亚铁溶液中通入氯气的离子反应为2Fe2++Cl2═2Fe3++2Cl-,故C错误;
D.将铁粉加入稀硫酸中的离子反应为Fe+2H+═Fe2++H2↑,故D错误;
故选A.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应、离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应中电子、电荷守恒判断,题目难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
14.下列烷烃的系统命名中,不正确的是( )
| A. | 3,4-二甲基戊烷 | B. | 2,3-二甲基丁烷 | ||
| C. | 2,2-二甲基丁烷 | D. | 2,2,3,3-四甲基丁烷 |
11.下列叙述正确的是( )
| A. | 标准状况下,相同体积的SO2和SO3,质量比为4:5 | |
| B. | 相同状况下,质量相同的O2和O3,密度之比为3:2 | |
| C. | 相同质量的金刚石和石墨含有相同的C原子数和共价键数 | |
| D. | 标准状况下,相同体积的C2H2和C2H4,密度比为13:14 |
18.以下是对某水溶液进行SO42-离子检验的方法和结论,其中正确的是( )
| A. | 加入BaCl2溶液,产生了白色沉淀.则溶液中一定含有SO42- | |
| B. | 加入BaCl2溶液产生了白色沉淀,再加盐酸,沉淀不消失,则溶液中一定含有SO42- | |
| C. | 加入盐酸酸化的氯化钡溶液,产生白色沉淀,则溶液中一定有SO42- | |
| D. | 加入盐酸,溶液无明显现象,再加BaCl2溶液,产生了白色沉淀.则溶液中一定含有SO42- |
12.当光束通过下列分散系是,可能产生丁达尔效应的是( )
| A. | NaCl 溶液 | B. | Fe(OH)3 胶体 | C. | 盐酸 | D. | 蔗糖溶液 |
10.下列叙述正确的是( )
| A. | 中和热测定实验用的小烧杯和物质的量浓度溶液配制用的容量瓶都必须干燥 | |
| B. | 用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液,若滴定终点时仰视读数,测得氢氧化钠浓度偏低 | |
| C. | 配制2.0 mol•L-1的硫酸,若定容时俯视,则所得溶液浓度偏高(其他操作均正确) | |
| D. | 用铜电极电解2.0 mol•L-1的硫酸,阴阳两极生成气体的体积之比为2:1 |
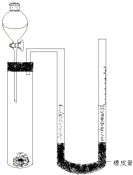 在化学研究领域,经常需要对一些物质进行性质的确定.如利用下列装置(夹持仪器已略去)测出一定质量镁与盐酸反应放出的气体体积,对金属镁的相对原子质量进行测定,实验步骤如下:
在化学研究领域,经常需要对一些物质进行性质的确定.如利用下列装置(夹持仪器已略去)测出一定质量镁与盐酸反应放出的气体体积,对金属镁的相对原子质量进行测定,实验步骤如下: