题目内容
下列根据实验操作和现象所得出的结论正确的是( )
| 实验操作 | 现象 | 解释或结论 | |
| A | 向溶液X中先滴加稀硝酸,再滴加Ba(NO3)2溶液 | 出现白色沉淀 | 溶液X中一定含有SO42- |
| B | 等体积pH=3的HA和HB两种酸分别与足量的锌反应,排水法收集气体 | HA放出的氢气多且反应速率快 | HB酸性比HA强 |
| C | 在镁、铝为电极,氢氧化钠为电解质的原电池装置中 | 镁表面有气泡 | 金属活动性:Al>Mg |
| D | 向1mL 1%的NaOH溶液中加入2mL 2%的CuSO4溶液,振荡后加入0.5mL有机物Y加热 | 未出现砖红色沉淀 | Y中不含有醛基 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价,硫酸根离子的检验,有机物(官能团)的检验,比较弱酸的相对强弱的实验
专题:实验评价题
分析:A.先滴加稀硝酸,可将亚硫酸根离子氧化;
B.等体积pH=3的HA和HB两种酸分别与足量的锌反应,HA放出气体多,则HA的浓度大;
C.镁、铝为电极,氢氧化钠为电解质的原电池装置中,Al为负极;
D.向1mL 1%的NaOH溶液中加入2mL 2%的CuSO4溶液,碱不足.
B.等体积pH=3的HA和HB两种酸分别与足量的锌反应,HA放出气体多,则HA的浓度大;
C.镁、铝为电极,氢氧化钠为电解质的原电池装置中,Al为负极;
D.向1mL 1%的NaOH溶液中加入2mL 2%的CuSO4溶液,碱不足.
解答:
解:A.先滴加稀硝酸,可将亚硫酸根离子氧化,则再滴加Ba(NO3)2溶液生成硫酸钡白色沉淀,原溶液中可能含亚硫酸根离子,或硫酸根离子或二者均存在,故A错误;
B.等体积pH=3的HA和HB两种酸分别与足量的锌反应,HA放出气体多,则HA的浓度大,HA为弱酸,所以酸性HB>HA,故B正确;
C.镁、铝为电极,氢氧化钠为电解质的原电池装置中,Al为负极,Mg为正极,氢离子在Mg电极上得到电子生成氢气,但金属性Mg>Al,Mg与NaOH不反应,故C错误;
D.向1mL 1%的NaOH溶液中加入2mL 2%的CuSO4溶液,碱不足,而检验有机物中含-CHO应在碱性条件下,所以实验失败,故D错误;
故选B.
B.等体积pH=3的HA和HB两种酸分别与足量的锌反应,HA放出气体多,则HA的浓度大,HA为弱酸,所以酸性HB>HA,故B正确;
C.镁、铝为电极,氢氧化钠为电解质的原电池装置中,Al为负极,Mg为正极,氢离子在Mg电极上得到电子生成氢气,但金属性Mg>Al,Mg与NaOH不反应,故C错误;
D.向1mL 1%的NaOH溶液中加入2mL 2%的CuSO4溶液,碱不足,而检验有机物中含-CHO应在碱性条件下,所以实验失败,故D错误;
故选B.
点评:本题考查化学实验方案的评价,为高频考点,涉及离子的检验、酸性比较及pH与浓度的关系、原电池、醛基检验等,把握化学反应原理及实验中细节为解答的关键,注意实验操作的可行性、评价性分析,题目难度不大.

练习册系列答案
相关题目
下列各组物质用括号内试剂加以鉴别,其中不合理的是( )
| A、Na2CO3溶液和Na2SO4溶液(稀盐酸) |
| B、CO2和H2(澄清石灰水) |
| C、NH4Cl溶液和(NH4)2SO4溶液(氢氧化钡溶液) |
| D、Na2CO3溶液和NaHCO3溶液(氢氧化钙溶液) |
下列化合物中同分异构体数目最少的是( )
| A、戊烷 | B、戊醇 |
| C、戊烯 | D、乙酸乙酯 |
下列试剂中,标签上应标注 和
和 的是( )
的是( )
 和
和 的是( )
的是( )| A、C2H5OH |
| B、HNO3 |
| C、NaOH |
| D、HCl |
M3+有2个电子层,则M在元素周期表中的位置是( )
| A、第2周期0族 |
| B、第2周期Ⅷ族 |
| C、第3周期ⅢA族 |
| D、第3周期ⅡA族 |
雾霾严重影响人们的生活与健康,某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-.某同学收集了该地区的雾霾,经必要的预处理后的试样溶液,设计并完成了如下实验:
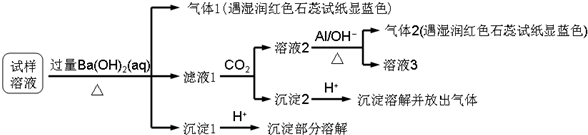
已知:3NO3-+8Al+5OH-+2H2O
3NH3↑+8AlO2-
根据以上的实验操作和现象,该同学得出的结论不正确的是( )

已知:3NO3-+8Al+5OH-+2H2O
| △ |
根据以上的实验操作和现象,该同学得出的结论不正确的是( )
| A、试样中肯定存在NH4+、Mg2+、SO42-和NO3- |
| B、试样中一定不含Al3+ |
| C、试样中可能存在Na+、Cl- |
| D、该雾霾中可能存在NaNO3、NH4Cl和MgSO4 |
下列叙述不正确的是( )
| A、Na、Mg、Al最外层电子数依次增多,其单核离子的氧化性依次增强 |
| B、N、O、F最高正价依次升高,对应的气态氢化物的稳定性依次增强 |
| C、第三周期元素的原子半径中,位于ⅦA族元素的最小 |
| D、Na、Mg、Al三种元素对应的氢氧化物的碱性依次减弱 |
下列关于乙醇的说法不正确的是( )
| A、可用纤维素的水解产物制取 |
| B、可由乙烯通过加成反应制取 |
| C、与乙醛互为同分异构体 |
| D、通过取代反应可制取乙酸乙酯 |