题目内容
7.如表实验操作或原理正确的是( )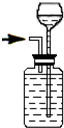 | 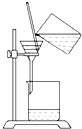 | 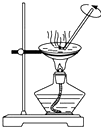 | 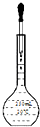 |
| A.检查气密性 | B.提纯Fe(OH)3胶体 | C.分离CCl4中的I2 | D.定容 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.通过气体发生器与液体构成封闭体系,依据改变体系内压强时产生的现象(如气泡的生成、水柱的形成、液面的升降等)来判断装置气密性的好坏;
B.溶液和胶体能透过滤纸;
C.四氯化碳和碘单质的沸点不同;
D.胶头滴管不能插入容量瓶内.
解答 解:A.通入气体,若漏斗下端升起一端液柱,说明气密性良好,故A正确;
B.溶液和胶体能透过滤纸,应用渗析提纯,故B错误;
C.四氯化碳和碘单质的沸点不同,应用蒸馏分离,故C错误;
D.胶头滴管不能插入容量瓶内,应悬于上方,以免污染试剂,故D错误.
故选A.
点评 本题考查较为综合,涉及基础实验操作,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握实验的方法、步骤和使用的仪器,注重相关基础知识的积累,难度不大.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
17.设NA为阿伏加德罗常数的值,对反应:
①CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1=-a kJ/mol
②CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H2=-b kJ/mol
(a、b均为正值),其他数据如表所示:
下列说法正确的是( )
①CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1=-a kJ/mol
②CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H2=-b kJ/mol
(a、b均为正值),其他数据如表所示:
| 化学键 | C=O | O=O | C-H | O-H |
| 键能/kJ•mol-1 | 798 | x | 413 | 463 |
| A. | H2O(g)═H2O(l)△S<0,△H=(a-b)kJ/mol | |
| B. | 当有4NA个C-H键断裂时,该反应放出热量一定为a kJ | |
| C. | x=$\frac{1796-b}{2}$ | |
| D. | 利用反应①设计的原电池电解精炼铜时,当负极输出0.2NA个电子时,电解槽的阳极一定减轻6.4g |
15.下列有关离子方程式的书写正确的是( )
| A. | Na2CO3溶液使酚酞变红:CO32-+H2O═CO2↑+2OH- | |
| B. | AgCl悬浊液中滴加KI溶液:AgCl+I-?AgI+Cl- | |
| C. | CH3COOH溶液使石蕊试液变红:CH3COOH═CH3COO-+H+ | |
| D. | 用惰性电极电解CuSO4溶液的阴极反应式:4OH--4e-═2H2O+O2↑ |
2.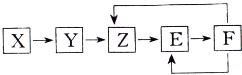 下列常见物质X、Y、Z、E、F均含有同一元素M,它们在一定条件下有如图所示的转化关系,已知Z为NO,以下有关这五种物质的推断中合理的是( )
下列常见物质X、Y、Z、E、F均含有同一元素M,它们在一定条件下有如图所示的转化关系,已知Z为NO,以下有关这五种物质的推断中合理的是( )
 下列常见物质X、Y、Z、E、F均含有同一元素M,它们在一定条件下有如图所示的转化关系,已知Z为NO,以下有关这五种物质的推断中合理的是( )
下列常见物质X、Y、Z、E、F均含有同一元素M,它们在一定条件下有如图所示的转化关系,已知Z为NO,以下有关这五种物质的推断中合理的是( )| A. | X一定含有氮元素,可能是单质也可能是化合物 | |
| B. | X→Y一定是氧化还原反应 | |
| C. | 常温下F与碳单质反应可能生成Z | |
| D. | 若X为单质,Y→Z可能属于化合反应 |
19.解释下列现象的化学用语正确的是( )
| A. | 铁钉在空气中出现红色的铁锈,其负极反应式为:Fe-3e-═Fe3+ | |
| B. | 氢氧化镁白色沉淀溶于氯化铵溶液:Mg(OH)2+NH4+═Mg2++NH3•H2O | |
| C. | 漂白粉溶液中加氯化亚铁溶液产生大量沉淀:Fe2++2ClO-+2H2O═Fe(OH)2↓+2HClO | |
| D. | 向足量铝粉与稀盐酸反应后的溶液中滴加碳酸氢钠溶液:3HCO3-+Al3+═Al(OH)3↓+3CO2↑ |
16.类推的思维方法在化学学习与研究中有时会产生错误结论,因此类推的结论最终要经过实践的检验,才能决定其正确与否.下列各组类推结论与描述对应正确的是( )
| 选项 | 反应I | 反应Ⅱ | 描述 |
| A | CuSO4+Fe- | CuSO4+Na- | 向CuSO4溶液中加入较活泼的金属单质均可以置换得到单质铜 |
| B | 浓氨水与浓盐酸 | 浓氨水与浓硝酸 | 在空气中靠近均能产生白烟 |
| C | NaOH+MgCl2- | NaOH+AlCl3- | 过量NaOH溶液加入溶液中均生成白色沉淀 |
| D | Ca(ClO)2+CO2- | Ca(ClO)2+SO2- | 向漂白粉溶液中通入足量的气体反应后,所得的溶液均具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
6.向下列各物质的水溶液中滴加稀硫酸或MgCl2溶液时,均有白色沉淀生成的是( )
| A. | BaCl2 | B. | KOH | C. | Na2CO3 | D. | Ba(OH)2 |
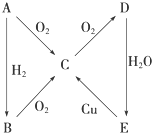 根据如图所示转化关系,判断A、B、C、D各是什么物质,写出有关反应的化学方程式:
根据如图所示转化关系,判断A、B、C、D各是什么物质,写出有关反应的化学方程式: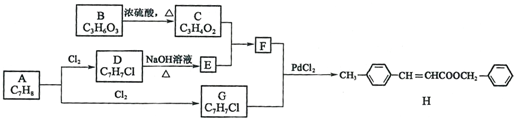
 .
. .
.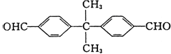 、
、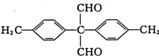 .
.