题目内容
7.某化学小组制备氢氧化铁胶体:洁净的小烧杯盛适量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入1mol•L-1FeCl3溶液,至液体呈透明的红褐色.回答下列问题:(1)氢氧化铁胶体中微粒直径的范围是1nm~100nm.生成红褐色胶体的方程式为FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl
(2)一位同学在实验过程中边滴加FeCl3溶液边搅拌,没有制得胶体,反而出现了浑浊,请帮他分析原因:搅拌使胶体发生聚沉而出现浑浊.
(3)如果向制得的氢氧化铁胶体中逐滴滴加盐酸至过量,操作过程中观察到的现象是:先出现浑浊后浑浊逐渐消失.
分析 (1)胶体粒子直径大小在1nm~100nm;FeCl3与水在加热条件下反应生成氢氧化铁胶体和氯化氢;
(2)搅拌能使胶体聚沉;
(3)氢氧化铁胶体先发生聚沉,然后盐酸溶液与氢氧化铁反应.
解答 解:(1)氢氧化铁胶体是胶体分散系中的一种,胶体粒子直径大小在1nm~100nm;生成红褐色胶体的反应为FeCl3与水在加热条件下生成氢氧化铁胶体和氯化氢,方程式为:FeCl3+3H2O $\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl,故答案为:1nm~100nm; FeCl3+3H2O $\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl;
(2)搅拌能使胶体聚沉,原因是搅拌能减弱胶粒对电荷的吸附能力,使胶粒容易碰撞结合成更大的颗粒而聚沉,故边滴加溶液边用玻璃棒搅拌,会导致制备胶体失败,故答案为:搅拌使胶体发生聚沉而出现浑浊;
(3)向Fe(OH)3胶体中逐滴滴加盐酸至过量,先胶体和电解质溶液产生聚沉现象,有沉淀生成,后氢氧化铁又和盐酸反应生成可溶性的氯化铁,所以沉淀又溶解,故答案为:先出现浑浊后浑浊逐渐消失.
点评 本题要求熟练掌握胶体的制备知识,题目难度不大,特别是氢氧化铁胶体的制备方程式是常考常错的内容,胶体的聚沉以及沉淀的溶解一直是具有一定综合性的热点.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
15. 某学生用0.100mol•L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分为如下几步:
某学生用0.100mol•L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分为如下几步:
A.移取20.00mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管使尖嘴处充满溶液;
D.取标准KOH溶液注入碱式滴定管至0刻度以上 2~3cm;
E.调节液面至0或0以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度.
就此实验完成下列问题:
(1)正确操作步骤的顺序是B、D、C、E、A、F(填字母序号).
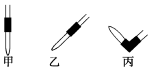
(2)如图,排除碱式滴定管中气泡的方法应采用操作丙(填图编号),轻轻挤压玻璃球使尖嘴部分充满碱液.
(3)上述B步骤操作的目的是防止滴定管内壁附着的水将标准溶液稀释而带来误差.
(4)上述A步骤操作之前,若先用待测溶液润洗锥形瓶,则滴定结果偏高(填“偏高”、“偏低”或“不变”).
(5)判断到达滴定终点的实验现象是滴入最后一滴KOH溶液,溶液由无色变为浅红色,且在半分钟内不褪色.
(6)重复上述滴定2~3次,记录数据如表:
根据表中数据,可计算出该盐酸的浓度约为0.09mol/L(保留两位小数).
 某学生用0.100mol•L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分为如下几步:
某学生用0.100mol•L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分为如下几步:A.移取20.00mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管使尖嘴处充满溶液;
D.取标准KOH溶液注入碱式滴定管至0刻度以上 2~3cm;
E.调节液面至0或0以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度.
就此实验完成下列问题:
(1)正确操作步骤的顺序是B、D、C、E、A、F(填字母序号).
(2)如图,排除碱式滴定管中气泡的方法应采用操作丙(填图编号),轻轻挤压玻璃球使尖嘴部分充满碱液.
(3)上述B步骤操作的目的是防止滴定管内壁附着的水将标准溶液稀释而带来误差.
(4)上述A步骤操作之前,若先用待测溶液润洗锥形瓶,则滴定结果偏高(填“偏高”、“偏低”或“不变”).
(5)判断到达滴定终点的实验现象是滴入最后一滴KOH溶液,溶液由无色变为浅红色,且在半分钟内不褪色.
(6)重复上述滴定2~3次,记录数据如表:
| 实验 编号 | KOH溶液的浓度(mol•L-1) | 滴定完成时,滴入KOH溶液的体积(mL) | 待测盐酸溶液的体积(mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
2.下列实验操作所用仪器合理的是( )
| A. | 把烧杯内的溶液转移到容量瓶中时,必须用玻璃棒引流 | |
| B. | 用100mL量筒量取95.20 mL盐酸 | |
| C. | 用托盘天平称取25.20gNaCl | |
| D. | 用500mL容量瓶配制50mL0.10mol/L溶液 |
12.下列反应中,不属于氧化还原反应的是( )
| A. | H2+F2═2HF | B. | 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2 | ||
| C. | NaOH+HCl═NaCl+H2O | D. | 4HNO3$\frac{\underline{\;\;△\;\;}}{\;}$ 2H2O+4NO2↑+O2↑ |
19.设NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 常温常压下,48gO3含有的氧原子数为3NA | |
| B. | 1 mol OH-所含的电子数为9NA | |
| C. | 常温常压下,11.2 L氧气所含的原子数为NA | |
| D. | 物质的量浓度为1mol/L MgCl2溶液,含有Cl-离子数为2NA |
16.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 32 g O2气体含有的氧原子数为NA | |
| B. | 2 L 0.3 mol/L Na2SO4溶液中含有Na+为0.6NA | |
| C. | 54 g铝完全反应后失去的电子数为6NA | |
| D. | 11.2 L氮气所含的分子数为0.5NA |
3. 氮可形成多种氧化物,如NO、NO2、N2O4等.
氮可形成多种氧化物,如NO、NO2、N2O4等.
(1)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH═NaNO3+NaNO2+H2O.含0.2mol NaOH的水溶液与 0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.1mol/L的 CH3COONa溶液,则两溶液中c(NO3-)、c(NO2-)和c(CH3COO-)由大到小的顺序为c(NO3-)>c(NO2-)>c(CH3COO-)(已知HNO2的电离常数Ka=7.1×10-4mol/L,CH3COOH的电离常数Ka=1.7×10-5mol/L).可使溶液A和溶液B的pH相等的方法是bc.
a.向溶液A中加适量水 b.向溶液A中加适量NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH
(2)100℃时,将0.400mol的NO2气体充入2L抽空的密闭容器中,发生反应2NO2(g)?N2O4(g)△H<0.每隔一定时间就对该容器内的物质进行分析,得到如表所示数据.
在上述条件下,从反应开始直至20s时,二氧化氮的平均反应速率为0.15mol/(L•min),n3=n4(填“>”“<”或“=”),该反应的平衡常数的值为2.8.若在相同条件下,最初向该容器充入的是N2O4气体,达到上述同样的平衡状态,则N2O4的起始浓度是0.1mol/L;假设从放入N2O4到平衡时需要80s,则达到平衡时四氧化二氮的转化率为60%.
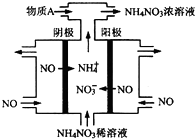
(3)电解NO制备NH4NO3,其工作原理如图所示,为使电解产物全部转化为NH4NO3,需补充物质A,A是NH3,理由是根据反应:8NO+7H2O$\frac{\underline{\;通电\;}}{\;}$3NH4NO3+2HNO3,电解产生的硝酸多,需补充NH3.
 氮可形成多种氧化物,如NO、NO2、N2O4等.
氮可形成多种氧化物,如NO、NO2、N2O4等.(1)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH═NaNO3+NaNO2+H2O.含0.2mol NaOH的水溶液与 0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.1mol/L的 CH3COONa溶液,则两溶液中c(NO3-)、c(NO2-)和c(CH3COO-)由大到小的顺序为c(NO3-)>c(NO2-)>c(CH3COO-)(已知HNO2的电离常数Ka=7.1×10-4mol/L,CH3COOH的电离常数Ka=1.7×10-5mol/L).可使溶液A和溶液B的pH相等的方法是bc.
a.向溶液A中加适量水 b.向溶液A中加适量NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH
(2)100℃时,将0.400mol的NO2气体充入2L抽空的密闭容器中,发生反应2NO2(g)?N2O4(g)△H<0.每隔一定时间就对该容器内的物质进行分析,得到如表所示数据.
| 时间/s | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
(3)电解NO制备NH4NO3,其工作原理如图所示,为使电解产物全部转化为NH4NO3,需补充物质A,A是NH3,理由是根据反应:8NO+7H2O$\frac{\underline{\;通电\;}}{\;}$3NH4NO3+2HNO3,电解产生的硝酸多,需补充NH3.