题目内容
1.表为元素周期表的一部分,请回答下列问题:| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ③ | |||||||
| 3 | ① | ② | ④ | ⑤ | ||||
(2)④和⑤两种元素的最高价氧化物对应水化物酸性较弱的是H2SO4(填化学式),②和④两种元素中,原子半径较大的是Al(填元素符号).
(3)元素①的氢氧化物与元素⑤的单质在常温下反应,化学方程式为:2NaOH+Cl2═NaCl+NaClO+H2O.
分析 由元素在周期表的位置可知,①~⑤分别为Na、Al、N、S、Cl,
(1)N的原子结构中有2个电子层,最外层电子数为5;
(2)非金属性越强,最高价氧化物对应水化物酸性越强;同周期从左向右原子半径减小;
(3)氯气与NaOH反应生成氯化钠、次氯酸钠和水.
解答 解:由元素在周期表的位置可知,①~⑤分别为Na、Al、N、S、Cl,
(1)元素③在元素周期表中的位置是第二周期VA族,故答案为:第二周期VA族;
(2)④和⑤两种元素的最高价氧化物对应水化物酸性较弱的是H2SO4,②和④两种元素中,原子半径较大的是Al,故答案为:H2SO4;Al;
(3)元素①的氢氧化物与元素⑤的单质在常温下反应,化学方程式为2NaOH+Cl2═NaCl+NaClO+H2O,故答案为:2NaOH+Cl2═NaCl+NaClO+H2O.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、元素周期律、元素化合物知识等为解答的关键,侧重分析与应用能力的考查,注意非金属性的应用,题目难度不大.

练习册系列答案
相关题目
12.下列实验描述正确的是( )
| A. | 向淀粉水解后的溶液中加入碘水,溶液变蓝色,证明淀粉没有水解 | |
| B. | 向NaOH溶液中滴加浓度均为0.1mol•L-1的FeCl3和AlCl3混合溶液,出现红褐色沉淀,由此可知Ksp[Fe(OH)3]<Ksp[Al(OH)3] | |
| C. | 向待测试样中加入过量稀盐酸无现象,再滴加BaCl2溶液,有白色沉淀生成,证明试样中含SO42- | |
| D. | 将Fe(NO3)2样品溶于稀硫酸,再滴加KSCN溶液变为红色,证明样品已部分或全部变质 |
12.下列有关原子结构和元素周期律表述正确的是( )
①ⅦA族元素是同周期中非金属性最强的元素
②原子序数为15的元素的最高化合价为+3
③第二周期ⅣA族元素的原子核电荷数和中子数一定为6
④原子序数为12的元素位于元素周期表的第三周期ⅡA族.
①ⅦA族元素是同周期中非金属性最强的元素
②原子序数为15的元素的最高化合价为+3
③第二周期ⅣA族元素的原子核电荷数和中子数一定为6
④原子序数为12的元素位于元素周期表的第三周期ⅡA族.
| A. | ①④ | B. | ①③ | C. | ②④ | D. | ③④ |
9.下列有关物质的组成与结构的说法正确的是( )
| A. | 1 mol 庚烷分子中含共价键 23 NA | |
| B. | 所有烷烃分子中均存在极性键和非极性键 | |
| C. | C2H4、C2H4Br2、CH2Cl2均只能代表一种物质 | |
| D. | A、B 两种烃,它们含碳质量分数相同,则 A 和 B 最简式一定相同 |
16.下列各选项中的离子可大量共存的是( )
| A. | H+、Na+、NO3-、CO32- | B. | Fe3+、K+、I-、SCN | ||
| C. | Al3-、Cu2+、SO42-、NO3- | D. | NH4-、K+、Cl-、OH- |
6.氢气还原氧化铜:CuO+H2 $\frac{\underline{\;\;△\;\;}}{\;}$ Cu+H2O,在该反应中( )
| A. | CuO作还原剂 | B. | 铜元素化合价降低 | ||
| C. | CuO作氧化剂 | D. | 铜元素被氧化 |
13.下列关于氯气的叙述正确的是( )
| A. | 钠在氯气中燃烧产生白色烟雾 | |
| B. | 氯气可以与铁反应,因此氯气不能贮藏在钢瓶中 | |
| C. | 纯净的氢气可以在氯气中安静地燃烧,发出苍白色火焰 | |
| D. | 氯气可用于漂白,这是氯气的漂白作用 |
10.下列各项中正确的是( )
| A. | 可用高锰酸钾溶液鉴别甲苯、环己烯与溴苯 | |
| B. | 淀粉与纤维素不互为同分异构体,但二者完全水解的产物相同 | |
| C. | 石油裂解和油脂皂化都是由高分子化合物生成小分子物质的过程 | |
| D. | 对苯二甲酸(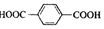 )与乙二醇(HOCH2CH2OH)能通过加聚反应制取聚醋纤维( )与乙二醇(HOCH2CH2OH)能通过加聚反应制取聚醋纤维(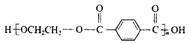 ) ) |
11.下列实验方案能达到实验目的是( )
| 选项 | 目的 | 实验方案 |
| A. | 比较Mg、Al的金属性 | 将去除氧化膜的镁条、铝片分别放入沸水中 |
| B. | 鉴别MgCl2和 AlCl3溶液 | 将过量稀氨水分别滴入MgCl2和 AlCl3溶液中 |
| C. | 证明苯环对羟基活性的影响 | 分别向苯和苯酚溶液中滴加饱和溴水 |
| D. | 比较浓度对反应速率的影响 | 将不同浓度的KMnO4溶液、稀H2SO4与同浓度的H2C2O4溶液混合 |
| A. | A | B. | B | C. | C | D. | D |