题目内容
9.关于某无色溶液中所含离子的鉴别,下列判断正确的是( )| A. | 加入AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有Cl-存在 | |
| B. | 加入盐酸,生成的气体能使澄清石灰水变浑浊,可确定有CO32-存在 | |
| C. | 加入Ba(NO3)2,生成白色沉淀,加稀盐酸沉淀不消失,可确定有SO42-存在 | |
| D. | 用洁净的铂丝蘸取溶液放在火焰上灼烧,观察到火焰呈黄色,可确定有Na+存在 |
分析 A.白色沉淀为AgCl或硫酸银等;
B.气体为二氧化碳或二氧化硫;
C.白色沉淀为硫酸钡,亚硫酸与硝酸钡发生氧化还原反应生成硫酸钡沉淀;
D.焰色反应为元素的性质,火焰呈黄色,可知溶液中一定含钠离子.
解答 解:A.白色沉淀为AgCl或硫酸银等,加稀盐酸沉淀不消失,原溶液中可能含氯离子或硫酸根离子,故A错误;
B.气体为二氧化碳或二氧化硫,则原溶液中可能含CO32-、SO32-、HCO3-等,故B错误;
C.白色沉淀为硫酸钡,加稀盐酸沉淀不消失,若原溶液为亚硫酸出现相同的现象,则原溶液中不一定含SO42-,故C错误;
D.焰色反应为元素的性质,火焰呈黄色,可知溶液中一定含钠离子,检验方法合理,故D正确;
故选D.
点评 本题考查常见离子的检验,为高频考点,把握白色沉淀及气体的判断、现象与结论的关系为解答的关键,侧重分析与实验能力的考查,注意离子检验中排除干扰离子,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.对于反应2A2+B2═2C来说,以下表示中,反应速率最快的是( )
| A. | v(B2)=3 mol/(L•min) | B. | v(A2)=4 mol/(L•min) | ||
| C. | v(C)=0.03 mol/(L•s) | D. | v(B2)=0.08 mol/(L•s) |
20.羧酸分子里的官能团是( )
| A. | 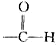 | B. | 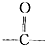 | C. | 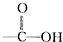 | D. | -CnHn+1 |
18.己知:KI溶液在酸性条件下能被空气中的O2氧化,反应的离子方程式为:O2+4I-+4H+═2I2+2H2O.
(I)某化学小组为探究不同条件对上述反应速率的影响,设计如下实验,完成表中①和②的内容.
(限选试剂:0.lmol/L硫酸、0.2mol/L硫酸、1mol/L KOH溶液、淀粉溶液)
(2)在上述实验中,三种溶液混合的顺序最合理的是C(选填下列选项);应记录的内容溶液从无色变为蓝色所需的时间.
A.先将硫酸溶液与淀粉溶液混合,然后再加入KI溶液
B.先将KI溶液与硫酸溶液混合,然后再加入淀粉溶液
C.先将KI溶液与淀粉溶液混合,然后再加入硫酸溶液
(3)在实验中,发现露置在空气中的KI溶液逐渐变黄色.通过查阅资料知:KI溶液在空气中会生成I2和KOH.小组同学对该描述有疑问:I2为何能与KOH共存?为此提出下列假设进行探究:
假设一:常温下,I2和KOH不反应
假设二:溶液碱性弱,I2和KOH不反应
假设三:…
请设计实验验证假设二,完成表中的内容
(限选试剂:1mol/L盐酸、1mol/L KOH溶液、碘水、淀粉溶液)
(I)某化学小组为探究不同条件对上述反应速率的影响,设计如下实验,完成表中①和②的内容.
(限选试剂:0.lmol/L硫酸、0.2mol/L硫酸、1mol/L KOH溶液、淀粉溶液)
| 组别 | 温度 | KI溶液 | H2SO4溶液 | 淀粉溶液 | 实验目的 | ||
| c(KI) | V | c(H2SO4) | V | ||||
| 1 | 298K | 1mol/L | 5mL | 0.1mol/L | 5mL | 3滴 | 1组和2组探究②0.2mol/L温度对该反应速率的影响;1组和3组探究反应物浓度对该反应速率的影响 |
| 2 | 308K | 1mol/L | 5mL | 0.1mol/L | 5mL | 3滴 | |
| 3 | 298K | 1mol/L | 5mL | ① | 5mL | 3滴 | |
A.先将硫酸溶液与淀粉溶液混合,然后再加入KI溶液
B.先将KI溶液与硫酸溶液混合,然后再加入淀粉溶液
C.先将KI溶液与淀粉溶液混合,然后再加入硫酸溶液
(3)在实验中,发现露置在空气中的KI溶液逐渐变黄色.通过查阅资料知:KI溶液在空气中会生成I2和KOH.小组同学对该描述有疑问:I2为何能与KOH共存?为此提出下列假设进行探究:
假设一:常温下,I2和KOH不反应
假设二:溶液碱性弱,I2和KOH不反应
假设三:…
请设计实验验证假设二,完成表中的内容
| 实验方案 | 预期实验现象与结论 |
| 取少量碘水于试管中,滴入几滴淀粉溶液,然后逐滴加入1mol/LKOH溶液,观察现象 | 若蓝色不褪色,则假设二正确 |

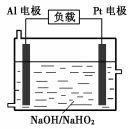 已知H2O2是一种弱酸,在强碱性溶液中主要以HO2-形式存在.目前研究比较热门的Al-H2O2燃料电池,其原理如图所示,电池总反应如下:
已知H2O2是一种弱酸,在强碱性溶液中主要以HO2-形式存在.目前研究比较热门的Al-H2O2燃料电池,其原理如图所示,电池总反应如下:
 (不考虑空间构型,如有配位键,请标出)
(不考虑空间构型,如有配位键,请标出)