题目内容
 某些金属及金属氧化物对H2O2的分解反应具有催化作用,请回答下列问题:
某些金属及金属氧化物对H2O2的分解反应具有催化作用,请回答下列问题:(1)已知:2H2O2(aq)=2H2O(l)+O2(g)的△H<0,则该反应的逆反应能否自发进行?
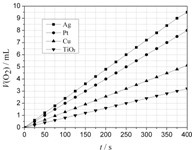
(2)某同学选用Ag、Pt、Cu、TiO2作为催化剂,在25℃时,保持其它实验条件相同,测得生成的O2体积(V).V与分解时间(t)的关系如图所示
(O2的体积已折算成标准状况),则:
①在不同催化剂存在下,H2O2分解反应的活化能大小顺序是 Ea
②金属Pt催化下,H2O2分解的反应速率v(O2)=
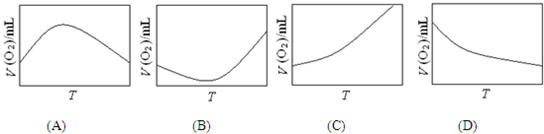
(3)为研究温度对H2O2分解速率的影响(不加催化剂),可将一定浓度和体积的H2O2置于密闭容器中,在某温度下,经过一定的时间t,测定生成O2的体积V.然后保持其它初始条件不变,改变温度T,重复上述实验.获得V(O2)~T关系曲线.下列趋势图最可能符合实测V(O2)~T关系曲线的是
(4)以Pt为电极电解H2O2也可产生氧气,写出H2O2水溶液电解过程中的电极反应式(已知:H2O2的氧化性及还原性均比H2O强):阴极
考点:反应热和焓变,催化剂的作用,电解原理,探究温度、压强对化学反应速率的影响
专题:基本概念与基本理论
分析:(1)反应的自发性是由熵变和焓变共同决定,若△H<0,△S>0,则一定能自发进行,若△H>0,△S<0,则一定不能自发进行,若△H<0,△S<0或△H>0,△S>0,是否自发和温度有关;
(2)活化能越小,反应越容易进行,反应速率越快,根据速率大小来确定活化能的大小;从图象可看出,400s时,Pt催化分解生成氧气8mL,物质的量为:
=3.57×10-4mol,根据要求计算速率;
(3)根据温度对反应速率的影响考虑;
(4)电解总反应式为:2H2O2
2H2O+O2↑,分析化合价变化,可知阳极过氧化氢失电子生成氧气,阴极过氧化氢得电子生成水,据此写电极反应式.
(2)活化能越小,反应越容易进行,反应速率越快,根据速率大小来确定活化能的大小;从图象可看出,400s时,Pt催化分解生成氧气8mL,物质的量为:
| 0.008L |
| 22.4L/mol |
(3)根据温度对反应速率的影响考虑;
(4)电解总反应式为:2H2O2
| ||
解答:
解:(1)2H2O2(aq)=2H2O(l)+O2(g)的△H<0,△S>0,则一定能自发进行,而逆反应的△H>0,△S<0,则一定不能自发进行;
故答案为:不能; 逆反应的△H>0,△S<0,因此在任何温度下都不能自发进行;
(2)①从图示看出,反应速率由快到慢的顺序为:Ag、Pt、Cu、TiO2,活化能越小,反应越容易进行,反应速率越快,故活化能由大到小顺序为:Ea(TiO2)>Ea(Cu)>Ea(Pt)>Ea(Ag);
故答案为:Ea(TiO2)>Ea(Cu)>Ea(Pt)>Ea(Ag);
②从图象可看出,400s时,Pt催化分解生成氧气8mL,物质的量为:
=3.57×10-4mol,则1s分解氧气:
=8.9×10-7mol/s;
故答案为:8.9×10-7;
(3)因该反应是不可逆反应,不考虑温度对平衡移动的影响.温度升高反应速率加快,因而经过相同反应时间后测得的O2体积随温度升高而增大,故C图象符合;
故答案为:C;因该反应是不可逆反应,不考虑温度对平衡移动的影响.温度升高反应速率加快,因而经过相同反应时间后测得的O2体积随温度升高而增大;
(4)电解总反应式为:2H2O2
2H2O+O2↑,分析化合价变化,可知阳极过氧化氢失电子生成氧气,反应式为:H2O2-2e-=O2↑+2H+,阴极过氧化氢得电子生成水,反应式为:H2O2+2H++2e-=2H2O,
故答案为:H2O2+2H++2e-=2H2O; H2O2-2e-=O2↑+2H+.
故答案为:不能; 逆反应的△H>0,△S<0,因此在任何温度下都不能自发进行;
(2)①从图示看出,反应速率由快到慢的顺序为:Ag、Pt、Cu、TiO2,活化能越小,反应越容易进行,反应速率越快,故活化能由大到小顺序为:Ea(TiO2)>Ea(Cu)>Ea(Pt)>Ea(Ag);
故答案为:Ea(TiO2)>Ea(Cu)>Ea(Pt)>Ea(Ag);
②从图象可看出,400s时,Pt催化分解生成氧气8mL,物质的量为:
| 0.008L |
| 22.4L/mol |
| 3.57×10-4mol |
| 400s |
故答案为:8.9×10-7;
(3)因该反应是不可逆反应,不考虑温度对平衡移动的影响.温度升高反应速率加快,因而经过相同反应时间后测得的O2体积随温度升高而增大,故C图象符合;
故答案为:C;因该反应是不可逆反应,不考虑温度对平衡移动的影响.温度升高反应速率加快,因而经过相同反应时间后测得的O2体积随温度升高而增大;
(4)电解总反应式为:2H2O2
| ||
故答案为:H2O2+2H++2e-=2H2O; H2O2-2e-=O2↑+2H+.
点评:本题考查了化学反应的方向性、影响反应速率的因素及速率的计算、电解原理等,中等难度.注意本题中反应速率不是浓度变化与时间之比,而是物质的量变化与时间之比,要根据题给信息作相应的调整.

练习册系列答案
相关题目
已知有机物A的结构简式为 ,可发生硝化反应,则产生的一硝基化合物可能有( )
,可发生硝化反应,则产生的一硝基化合物可能有( )
 ,可发生硝化反应,则产生的一硝基化合物可能有( )
,可发生硝化反应,则产生的一硝基化合物可能有( )| A、4种 | B、5种 | C、6种 | D、7种 |
NA代表阿伏加德罗常数,下列说法错误的是( )
| A、标准状况下,22.4L NO和22.4L O2的混合,混合气体中含有的氧原子数为3NA | ||||
| B、0.012kg 13C中,含中子数为7NA | ||||
| C、25℃时,1L pH=13的氢氧化钡溶液中含有0.1NA个氢氧根离子 | ||||
D、在反应3SiO2+6C+2N2
|
有A、B、C、D、E、F六种短周期元素,原子序数依次增大.已知A的一种核素的原子核为质子,B原子的最外层电子数是次外层电子数的2倍.B原子的最外层电子数是D、E原子最外层电子数之和,C原子的最外层电子数是D、F原子最外层电子数之和.下列推论不正确的是( )
| A、A、B两元素能形成多种化合物 |
| B、D、E两元素的最高价氧化物对应的水化物可相互反应 |
| C、C的气态氢化物的稳定性一定大于F的气态氢化物 |
| D、C、F两种元素可以形成化合物 |
NA为阿伏加德罗常数,下列物质的物质的量最小的是( )
| A、含NA个氧原子的O2 |
| B、标准状况下2.24LN2 |
| C、0.5molCH4 |
| D、22gCO2(CO2摩尔质量为44g?mol-1) |
A是合成天然橡胶的单体,分子式为C5H8. 下列说法错误的是( )
A、A的结构简式为: |
| B、A→天然橡胶的反应类型为加聚反应 |
| C、天然橡胶属于线型高分子化合物 |
| D、天然橡胶具有热固性 |

