题目内容
Al及其化合物用途广泛,工业上可以将明矾石经处理后得到明矾[KAl(SO4)2?12H2O],再将明矾焙烧后制得Al2O3等物质,进一步处理后还可以得到Al.
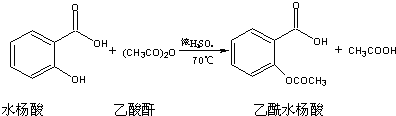
已知焙烧明矾的化学方程式为:4KAl(SO4)2?12H2O+3S
2J2SO4+2Al2O3+9SO2↑+48H2O
请回答:
(1)Al2O3的摩尔质量是 .
(2)工业上可用电解Al2O3制备Al,其化学方程式是 .
(3)在焙烧明矾的反应中,氧化剂和还原剂的物质的量之比是 .
(4)焙烧明矾时产生的SO2可综合利用来制硫酸.
已知25℃、101kPa时:
2SO2(g)+O2(g)?2SO3(g)△H1=一197kJ/mol
2H2O (g)=2H2O(1)△H2=一44kJ/mol
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l)△H3=一545kJ/mol
SO3 (g)与H2O(l)反应的热化学方程式是 .
(5)以Al和NiO(OH)为电极,NaOH溶液为电解液可以组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2.
①该电池的负极反应式 .
②电池总反应的化学方程式 .
已知焙烧明矾的化学方程式为:4KAl(SO4)2?12H2O+3S
| ||
请回答:
(1)Al2O3的摩尔质量是
(2)工业上可用电解Al2O3制备Al,其化学方程式是
(3)在焙烧明矾的反应中,氧化剂和还原剂的物质的量之比是
(4)焙烧明矾时产生的SO2可综合利用来制硫酸.
已知25℃、101kPa时:
2SO2(g)+O2(g)?2SO3(g)△H1=一197kJ/mol
2H2O (g)=2H2O(1)△H2=一44kJ/mol
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l)△H3=一545kJ/mol
SO3 (g)与H2O(l)反应的热化学方程式是
(5)以Al和NiO(OH)为电极,NaOH溶液为电解液可以组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2.
①该电池的负极反应式
②电池总反应的化学方程式
考点:用盖斯定律进行有关反应热的计算,摩尔质量,氧化还原反应,原电池和电解池的工作原理,金属冶炼的一般原理
专题:
分析:(1)根据摩尔质量在数值上等于其相对分子质量;
(2)工业上可用电解熔融Al2O3制备Al;
(3)该反应中,S元素的化合价由0价和+6价变为+4价,得电子的反应物是氧化剂,失电子的反应物是还原剂;
(4)依据热化学方程式和盖斯定律计算得到;
(5)以Al的单质和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,Al在负极失去电子,碱性条件下生成偏铝酸钠来书写;
(2)工业上可用电解熔融Al2O3制备Al;
(3)该反应中,S元素的化合价由0价和+6价变为+4价,得电子的反应物是氧化剂,失电子的反应物是还原剂;
(4)依据热化学方程式和盖斯定律计算得到;
(5)以Al的单质和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,Al在负极失去电子,碱性条件下生成偏铝酸钠来书写;
解答:
解:(1)根据摩尔质量在数值上等于其相对分子质量,则Al2O3的摩尔质量是102 g/mol,故答案为:102 g/mol;
(2)工业上可用电解熔融Al2O3制备Al,方程式为:2Al2O3(熔融)
4Al+3O2↑,故答案为:2Al2O3(熔融)
4Al+3O2↑;
(3)4KAl(SO4)2?12H2O+3S
2J2SO4+2Al2O3+9SO2↑+48H2O,该反应中,S元素的化合价由0价和+6价变为+4价,所以部分4KAl(SO4)2?12H2O作氧化剂(6个硫酸根被还原,2个硫酸根保持不变),硫作还原剂,还原剂和氧化剂的物质的量之比为6:3=2:1,故答案为:2:1;
(4)2SO2(g)+O2(g)?2SO3(g)△H1=-197kJ/mol;Ⅰ
H2O(g)?H2O(l)△H2=-44kJ/mol;Ⅱ
2SO2(g)+O2(g)+2H2O(g)═2H2SO4(l)△H3=-545kJ/mol.Ⅲ
依据盖斯定律Ⅲ-Ⅰ-2×Ⅱ得到:2SO3(g)+2H2O(l)=2H2SO4(l)△H=-260KJ/mol;
即反应的热化学方程式为:SO3(g)+H2O(l)=H2SO4(l)△H=-130KJ/mol;
故答案为:SO3(g)+H2O(l)=H2SO4(l)△H=-130KJ/mol;
(5)以Al的单质和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,Al在负极失去电子,碱性条件下生成偏铝酸钠,电极方程式为:Al-3e-+4OH-=AlO2-+2H2O;该电池总反应的化学方程式是:Al+3NiO(OH)+H2O+NaOH═NaAlO2+3Ni(OH)2,
故答案为:Al-3e-+4OH-=AlO2-+2H2O;Al+3NiO(OH)+H2O+NaOH═NaAlO2+3Ni(OH)2.
(2)工业上可用电解熔融Al2O3制备Al,方程式为:2Al2O3(熔融)
| ||
| 冰晶石 |
| ||
| 冰晶石 |
(3)4KAl(SO4)2?12H2O+3S
| ||
(4)2SO2(g)+O2(g)?2SO3(g)△H1=-197kJ/mol;Ⅰ
H2O(g)?H2O(l)△H2=-44kJ/mol;Ⅱ
2SO2(g)+O2(g)+2H2O(g)═2H2SO4(l)△H3=-545kJ/mol.Ⅲ
依据盖斯定律Ⅲ-Ⅰ-2×Ⅱ得到:2SO3(g)+2H2O(l)=2H2SO4(l)△H=-260KJ/mol;
即反应的热化学方程式为:SO3(g)+H2O(l)=H2SO4(l)△H=-130KJ/mol;
故答案为:SO3(g)+H2O(l)=H2SO4(l)△H=-130KJ/mol;
(5)以Al的单质和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,Al在负极失去电子,碱性条件下生成偏铝酸钠,电极方程式为:Al-3e-+4OH-=AlO2-+2H2O;该电池总反应的化学方程式是:Al+3NiO(OH)+H2O+NaOH═NaAlO2+3Ni(OH)2,
故答案为:Al-3e-+4OH-=AlO2-+2H2O;Al+3NiO(OH)+H2O+NaOH═NaAlO2+3Ni(OH)2.
点评:本题考查了氧化还原反应概念分析判断,热化学方程式和盖斯定律的计算,原电池反应的方程式的书写,题目难度中等.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
只用下列试剂中的一种就能鉴别BaCl2、Na2CO3、K2SO4三种溶液,则该试剂是( )
| A、KCl溶液 |
| B、NaOH溶液 |
| C、稀H2SO4 |
| D、Na2SO4溶液 |
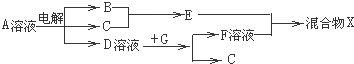
强酸性溶液X中可能含有Na+、K+、NH4+、Fe2+、A13+、CO32-、SO32-、SO42-、C1-中的若干种,某同学为了确认其成分,取X溶液进行连续实验,实验过程及产物如下:下列结论正确的是( )


| A、X中不能确定的离子是 A13+、Na+、K+和C1- |
| B、气体F经催化氧化可直接生成气体D |
| C、沉淀C一定是BaSO4、沉淀G一定是Fe(OH)3、沉淀I一定是Al(OH )3 |
| D、X中肯定存在Na+、Fe2+、A13+、NH4+、SO42- |
下列关于同分异构体、同系物、同素异形体、同位素的说法中错误的是( )
| A、乙酸与甲酸甲酯互为同分异构体 | ||||
B、
| ||||
| C、氧气与臭氧互为同素异形体 | ||||
| D、乙烯与聚乙烯互为同系物 |
甲、乙两物质的溶解度曲线如图所示,下列说法正确的是( )
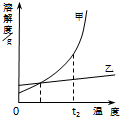

| A、t1℃时,物质的量浓度:甲=乙 |
| B、温度变化相同时,溶解度数值的变化量:甲>乙 |
| C、t2℃时,饱和溶液中溶质的质量分数:甲=乙 |
| D、相同质量的饱和溶液由t2℃降到t1℃时,析出的固体:甲<乙 |