题目内容
11.有关中和滴定有如下操作:①洗涤;②往滴定管内注入标准溶液;③滴定;④检查滴定管是否漏水;⑤用标准溶液润洗滴定管.其正确的操作顺序是( )| A. | ⑤①②④③ | B. | ⑤①②④③ | C. | ⑤②①④③ | D. | ④①⑤②③ |
分析 滴定操作中,首先需要检漏,然后洗涤仪器、润洗滴定管,再向滴定管中装入溶液,最后进行滴定,据此对各操作进行排序.
解答 解:中和滴定的操作步骤为:④检查滴定管是否漏水、①洗涤、⑤用标准溶液润洗滴定管、②往滴定管内注入标准溶液、③滴定,所以正确的滴定顺序为:④①⑤②③,
故选D.
点评 本题考查中和滴定操作方法,题目难度不大,注意把握常见化学实验的原理、步骤、方法以及注意事项,明确中和滴定操作方法为解答关键,试题培养了学生的分析能力及化学实验能力.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
2. 甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响.设计实验如下(所取溶液体积均为10mL):
甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响.设计实验如下(所取溶液体积均为10mL):
(1)其他条件不变时:探究温度对化学反应速率的影响,应选择①④(填实验编号).
(2)Na2S2O3和H2SO4反应的化学方程式为Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O.乙同学在实验室用Na2S2O3标液测量废水Ba2+的浓度,过程如下:(已知:2S2O32一+I2=S4O62-+2I-)
取废水25.0mL$→_{过滤}^{足量K_{2}CrO_{4}溶液}$BaCrO4固体$→_{稀HCl}^{过量HI}$I2、Cr3+、Ba2+、Cl-$\stackrel{Na_{2}S_{2}O_{3}}{→}$终点
(3)写出BaCrO4沉淀与过量HI、HCl溶液反应的离子方程式2BaCrO4+6I-+16H+=3I2+2Cr3++2Ba2++8H2O;
(4)以淀粉为指示剂,则到达滴定终点的现象是滴入最后一滴溶液,锥形瓶内溶液有蓝色变为无色,且30s内不复原;
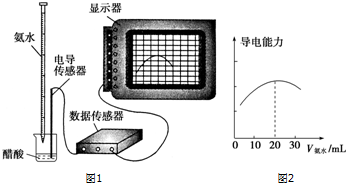
(5)若标液Na2S2O3的浓度0.0030mol•L-1,消耗该Na2S2O3溶液体积如图,则废水Ba2+的浓度为0.0011mol/L(保留两位有效数字).
 甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响.设计实验如下(所取溶液体积均为10mL):
甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响.设计实验如下(所取溶液体积均为10mL):| 实验编号 | 实验温度/℃ | c(Na2S2O3)/mol•L-1 | c(H2SO4)/mol•L-1 |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.1 | 0.2 |
| ③ | 50 | 0.2 | 0.1 |
| ④ | 50 | 0.1 | 0.1 |
(2)Na2S2O3和H2SO4反应的化学方程式为Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O.乙同学在实验室用Na2S2O3标液测量废水Ba2+的浓度,过程如下:(已知:2S2O32一+I2=S4O62-+2I-)
取废水25.0mL$→_{过滤}^{足量K_{2}CrO_{4}溶液}$BaCrO4固体$→_{稀HCl}^{过量HI}$I2、Cr3+、Ba2+、Cl-$\stackrel{Na_{2}S_{2}O_{3}}{→}$终点
(3)写出BaCrO4沉淀与过量HI、HCl溶液反应的离子方程式2BaCrO4+6I-+16H+=3I2+2Cr3++2Ba2++8H2O;
(4)以淀粉为指示剂,则到达滴定终点的现象是滴入最后一滴溶液,锥形瓶内溶液有蓝色变为无色,且30s内不复原;
(5)若标液Na2S2O3的浓度0.0030mol•L-1,消耗该Na2S2O3溶液体积如图,则废水Ba2+的浓度为0.0011mol/L(保留两位有效数字).
19.硫代硫酸钠俗称保险粉,又名“大苏打”.可用于照相业作定影剂、纸浆漂白作脱氯剂,也可用于氰化物、砷、汞、铅、铋、碘等中毒的治疗,也是一种常用的实验试剂.
I.已知:Na2S2O3+H2SO4=Na2SO4+S↓+SO2+H2O,某研究小组依据该反应探究外界条件对反应速率的影响,设计实验如下:
下列有关说法正确的是AD
A.实验①和②究其他条件不变时Na2S2O3浓度对相关反应速率的影响
B.实验①和③溶液变浑浊的时间相同
C.其他条件不变时,探究温度对化学反应速率的影响,应选择实验③和⑤
D.该同学在实验中采用的研究方法是实验比较法.
I.已知:Na2S2O3+H2SO4=Na2SO4+S↓+SO2+H2O,某研究小组依据该反应探究外界条件对反应速率的影响,设计实验如下:
| 实验 编号 | 实验温度 /℃ | Na2S2O3 | H2SO4 | 蒸馏水体积 /mL | ||
| 体积/mL | 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | |||
| ① | 25 | 10 | 0.1 | 10 | 0.1 | 0 |
| ② | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
| ③ | 25 | 5 | 0.2 | 10 | 0.2 | 5 |
| ④ | 50 | 5 | 0.1 | 10 | 0.1 | 5 |
| ⑤ | 50 | 10 | 0.2 | 5 | 0.2 | 5 |
A.实验①和②究其他条件不变时Na2S2O3浓度对相关反应速率的影响
B.实验①和③溶液变浑浊的时间相同
C.其他条件不变时,探究温度对化学反应速率的影响,应选择实验③和⑤
D.该同学在实验中采用的研究方法是实验比较法.
16.下列叙述正确的是( )
| A. | 用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2 | |
| B. | 在原电池的负极和电解池的阴极上都是发生失电子的氧化反应 | |
| C. | 用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH | |
| D. | 镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
3.我国科学家通过测量SiO2中26Al和10Be两种元素的比例来确定“北京人”年龄,这种测量方法叫铝铍测年法.关于26Al和10Be的说法不正确的是( )
| A. | 10Be和9Be是中子数不同质子数相同的不同原子 | |
| B. | 10Be的原子核内中子数比质子数多 | |
| C. | 5.2g 26Al3+中所含的电子数约为6.02×1024 | |
| D. | 26Al和26Mg的质子数和核外电子数均不相同,中子数相同 |
20.Se是人体必需微量元素,下列关于${\;}_{34}^{78}Se$和${\;}_{34}^{80}Se$的说法不正确的是( )
| A. | ${\;}_{34}^{78}Se$和${\;}_{34}^{80}Se$互为同素异形体 | |
| B. | ${\;}_{34}^{78}Se$和${\;}_{34}^{80}Se$电子数相同 | |
| C. | ${\;}_{34}^{78}Se$和${\;}_{34}^{80}Se$分别含有44和46个中子 | |
| D. | ${\;}_{34}^{78}Se$和${\;}_{34}^{80}Se$互为同位素 |
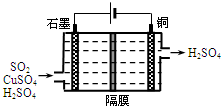 一种以铜作催化剂脱硫有如下两个过程:
一种以铜作催化剂脱硫有如下两个过程: