题目内容
下列说法中正确的是( )
| A、摩尔既是物质的数量单位又是物质的质量单位 |
| B、物质的量既表示物质的数量又表示物质的质量 |
| C、阿伏加德罗常数是12 kg 12C中含有的碳原子数目 |
| D、1 mol H2O中含有2 mol H原子和1mol O原子 |
考点:物质的量的单位--摩尔,阿伏加德罗常数
专题:化学用语专题
分析:A.摩尔为物质的量的单位,不是数量的单位;
B.物质的量描述的是一定数目的微观粒子的集体,表示的不是物质的质量;
C.阿伏伽德罗常数为12g12C中含有的碳原子数目;
D.根据水的分子组成及物质的量计算出含有的氢原子和氧原子的物质的量.
B.物质的量描述的是一定数目的微观粒子的集体,表示的不是物质的质量;
C.阿伏伽德罗常数为12g12C中含有的碳原子数目;
D.根据水的分子组成及物质的量计算出含有的氢原子和氧原子的物质的量.
解答:
解:A.摩尔只是物质的量的单位,不是物质的数量的单位,故A错误;
B.物质的量表示的是微观粒子的集体,不能表示物质的质量,故B错误;
C.碳原子的质量单位错误,应该是12g12C中含有的碳原子数目为阿伏伽德罗常数,故C错误;
D.水中含有2个氢原子和1个氧原子,1mol水中含有2mol氢原子、1mol氧原子,故D正确;
故选D.
B.物质的量表示的是微观粒子的集体,不能表示物质的质量,故B错误;
C.碳原子的质量单位错误,应该是12g12C中含有的碳原子数目为阿伏伽德罗常数,故C错误;
D.水中含有2个氢原子和1个氧原子,1mol水中含有2mol氢原子、1mol氧原子,故D正确;
故选D.
点评:本题考查了阿伏伽德罗常数的概念、物质的量与摩尔的概念及判断,题目难度不大,注意掌握物质的量与摩尔之间的关系,明确阿伏伽德罗常数的概念及标准.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
下列两种溶液,由水电离产生的c(H+)之比①:②是( )
①pH=1的盐酸; ②0.01mol/L的NaOH 溶液.
①pH=1的盐酸; ②0.01mol/L的NaOH 溶液.
| A、1:2 |
| B、1:10 |
| C、12:13 |
| D、1011:1 |
下列物质在一定条件下,可与CH4发生取代反应的是( )
| A、酸性高锰酸钾 | B、溴水 |
| C、氧气 | D、氯气 |
下列事实与胶体的性质有关的是( )
①用盐卤点豆腐 ②静电除尘 ③血液透析 ④江河入海口形成三角洲.
①用盐卤点豆腐 ②静电除尘 ③血液透析 ④江河入海口形成三角洲.
| A、只有①② | B、只有①②④ |
| C、只有①②③ | D、全部 |
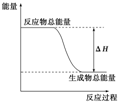 下列物质间的反应,其能量变化符合图的是( )
下列物质间的反应,其能量变化符合图的是( )| A、由氢气与氧气反应 |
| B、灼热的炭与二氧化碳反应 |
| C、Ba(OH)2?8H2O晶体和NH4Cl晶体混合 |
| D、碳酸钙的分解 |
在 2H2S+SO2═3S↓+2H2O 的反应中,被还原的元素是( )
| A、硫元素 | ||
| B、H2S中的硫元素 | ||
C、
| ||
D、
|
关于卤素(用X表示)的下列叙述,错误的是( )
| A、卤素单质与水反应均可用X2+H2O=HXO+HX表示 |
| B、HX都极易溶于水,它们的热稳定性随X的核电荷数的增加而减小 |
| C、卤素单质的颜色由F2→I2按相对分子质量增大而变深 |
| D、X-的还原性依次为:F-<Cl-<Br-<I- |
下列说法正确的是( )
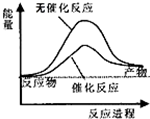

| A、如图可表示水分解过程中的能量变化 |
| B、高温高压下的超临界水,溶液中的氢离子和氢氧根离子浓度较大,有时显酸性,有时显碱性 |
| C、需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应 |
| D、等体积、等浓度的醋酸钠溶液和次氯酸钠溶液中,所含离子总数,前者小于后者 |
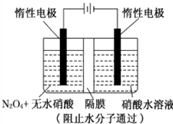 如图所示装置可通过发生“3N2O4+8HNO3=6N2O5+2NO+4H2O”制备N2O5,有关说法中错误的是( )
如图所示装置可通过发生“3N2O4+8HNO3=6N2O5+2NO+4H2O”制备N2O5,有关说法中错误的是( )| A、阴极的电极反应为:NO3-+4H++3e-=NO↑+2H2O |
| B、阳极的电极反应为:N2O4+2 HNO3-2e-=2N2O5+2H+ |
| C、当电路中通过6 mol e-时整个电解池中参与反应的HNO3为8mol |
| D、当电路中通过6 mol e-时,有8molH+从阳极向阴极迁移 |