题目内容
下列说法正确的是( )
| A、KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 |
| B、25℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,V(醋酸)<V(NaOH) |
| C、AgCl沉淀易转化成AgI沉淀且Ksp(AgX)=c(Ag+)?c(X-),故Ksp(AgI)<Ksp (AgCl) |
| D、BaSO4的水溶液不导电,故BaSO4是弱电解质 |
考点:电解质与非电解质,难溶电解质的溶解平衡及沉淀转化的本质
专题:基本概念与基本理论
分析:A.SO3的水溶液能导电,但SO3是非电解质;
B.醋酸溶液与NaOH溶液恰好反应时溶液呈碱性,若使溶液呈酸性,则酸过量;
C.根据沉淀转化原理:溶解度小的能转化为溶解度更小的;
D.硫酸钡是难溶的盐,熔融状态完全电离.
B.醋酸溶液与NaOH溶液恰好反应时溶液呈碱性,若使溶液呈酸性,则酸过量;
C.根据沉淀转化原理:溶解度小的能转化为溶解度更小的;
D.硫酸钡是难溶的盐,熔融状态完全电离.
解答:
解:A.SO3溶于水后和水反应生成硫酸,硫酸电离出阴阳离子而使其溶液导电,电离出阴阳离子的物质是硫酸而不是三氧化硫,所以SO3是非电解质,故A错误;
B.醋酸溶液与NaOH溶液恰好反应时溶液呈碱性,若使溶液呈酸性,则酸过量,用醋酸溶液滴定等浓度NaOH溶液至pH=7,V(醋酸)>V(NaOH),故B错误;
C.根据沉淀转化原理:溶解度小的能转化为溶解度更小的,所以AgCl沉淀易转化成AgI沉淀且Ksp(AgX)=c(Ag+)?c(X-),故Ksp(AgI)<Ksp (AgCl),故C正确;
D.硫酸钡是难溶的盐,熔融状态完全电离,所以BaSO4是强电解质,故D错误.
故选C.
B.醋酸溶液与NaOH溶液恰好反应时溶液呈碱性,若使溶液呈酸性,则酸过量,用醋酸溶液滴定等浓度NaOH溶液至pH=7,V(醋酸)>V(NaOH),故B错误;
C.根据沉淀转化原理:溶解度小的能转化为溶解度更小的,所以AgCl沉淀易转化成AgI沉淀且Ksp(AgX)=c(Ag+)?c(X-),故Ksp(AgI)<Ksp (AgCl),故C正确;
D.硫酸钡是难溶的盐,熔融状态完全电离,所以BaSO4是强电解质,故D错误.
故选C.
点评:本题主要考查了电解质、强电解质、沉淀转化原理、酸碱中和滴定,难度不大,注意知识的积累.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
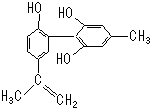 “人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )| A、1 mol该物质与浓溴水和H2反应最多消耗Br2和H2分别为4 mol、7 mol |
| B、滴入KMnO4(H+)溶液,观察紫色褪去,能证明结构中存在碳碳双键 |
| C、遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 |
| D、该分子中的所有原子可能共平面 |
下列关于油脂的叙述正确的是( )
| A、油脂有固定的熔、沸点 |
| B、油脂是高级脂肪酸的甘油酯 |
| C、油脂都不能使溴的四氯化碳溶液褪色 |
| D、油脂分成油和脂肪,油的熔点高于脂肪 |
已知H2(g)+Br2(l)→2HBr(g)+42kJ.1mol Br2(g)液化放出的能量为30kJ,其它相关数据如表:
则表格中的a值为( )
| H2(g) | Br2(g) | HBr(g) | |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | a | 369 |
| A、404 | B、344 |
| C、230 | D、200 |
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下11.2L的水中含有0.5个NA水分子 |
| B、22.4L N2的所含的电子数是14NA个 |
| C、氧化还原反应中,若消耗7.1g Cl2,必转移0.2NA个电子 |
| D、常温常压下,1mol N2和NO的混合气体中含2NA个原子 |
下列各组离子中,不能在溶液中大量共存的是( )
| A、H+、Cl-、Na+、SO42- |
| B、Mg2+、NO3-、K+、Br- |
| C、H+、Na+、Cl-、CO32- |
| D、OH-、NO3-、Na+、CO32- |
化学与人们的生活和健康密切相关,下列说法正确的是( )
| A、可以用淀粉检验加碘食盐中的碘元素 |
| B、鱼、肉、虾等食品用福尔马林防腐保鲜 |
| C、油脂可以提供能量,我们炒菜要多放油 |
| D、缺铁会产生贫血,常在酱油中补铁 |
下列物质中不会引起室内空气污染的是( )
| A、室内装潢涂料中释放出来的甲醛 |
| B、地砖中释放出的氡等放射性物质 |
| C、水果释放出的酯类物质 |
| D、厨房烧饭时产生的油烟 |